��Ŀ����
����Ŀ��������Ԫ��A��B��C��D��ԭ���������ε��������ǵĺ˵����֮��Ϊ32��ԭ������������֮��Ϊ10��A��Cͬ���壬B��Dͬ���壬A��Cԭ�ӵ�����������֮�͵���Bԭ�ӵĴ�����������������������ȷ����
A. DԪ�ش���Ԫ�����ڱ��е�3���ڵ���A��
B. ����Ԫ�ص�ԭ�Ӱ뾶��A<B<C<D
C. B��D�����������������Ƶ��������ʺͻ�ѧ����
D. һ�������£�B�������û���D���ʣ�C�������û���A����
���𰸡�D
��������
����A��Cͬ���壬A��Cԭ�ӵ�����������֮�͵���Bԭ�ӵĴ�������������A������������Ϊx����BΪ�ڶ�����Ԫ�أ���2x=2��x=1����AΪH��B��Dͬ���壬ԭ���������ε��������ǵĺ˵����֮��Ϊ32��ԭ������������֮��Ϊ10��BΪC��CΪNa��DΪSi�����ǵĺ˵����1+6+11+14=32���������⣻A�������3�����Ӳ㣬����������Ϊ4���������ڱ��еĵ������ڵ���A�壬��A����B�����Ӳ���Խ�࣬�뾶Խ����ͬһ���ڴ�����ԭ�Ӱ뾶�ڼ�С����뾶��ϵΪC��D��B��A����B����C��������̼�Ƿ��Ӿ��壬��������������ԭ�Ӿ��壬�������ʲ�ͬ����C����D����C+SiO2![]() Si+2CO����2Na+2H20�T2NaOH+H2������B�������û���D���ʣ�C�������û���A���ʣ���D��ȷ����ѡD��
Si+2CO����2Na+2H20�T2NaOH+H2������B�������û���D���ʣ�C�������û���A���ʣ���D��ȷ����ѡD��

 ������ϰ�ο����뵥Ԫ���ϵ�д�
������ϰ�ο����뵥Ԫ���ϵ�д� �����Ծ���ĩ���100��ϵ�д�
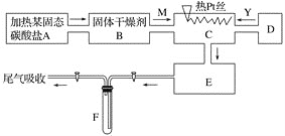
�����Ծ���ĩ���100��ϵ�д�����Ŀ��Ϊ̽��H2O2��SO2��Br2������ǿ����ijС��ͬѧ�������ʵ�飨�гּ�β������װ������ȥ���������Ѽ��飩��

ʵ����� | ʵ������ |
i����A�з�Һ©���������μ�Ũ���� | A�������ݲ�����B�к���ɫ��ˮ��ɫ��C���а�ɫ���� |
ii��ȡC�г����������� | C�а�ɫ�������ܽ� |
iii����B�з�Һ©����������εμ�H2O2 | ��ʼʱ��ɫ�����Ա仯�������μ�H2O2��Һ��һ��ʱ����Һ��ɺ���ɫ |
(1)C�в����İ�ɫ������______��
(2)��ͬѧͨ��C�в�����ɫ�������ó����ۣ������ԣ�H2O2��SO2��
����ͬѧ��Ϊ���ܵó��˽��ۣ���ʵ������˸Ľ���
���ɼУ�ͨ��N2�����ž�װ���ڿ����رյ��ɼУ��ٴ�A�з�Һ©���������˲�����Ŀ����_________________
�ڱ�ͬѧ�����˽�һ���ĸĽ���
��B��C֮������ʢ��CCl4��ϴ��ƿD����ͬѧ��Ŀ����______
�۽��Һͱ�ͬѧ�Ľ���ķ�������ʵ�飬C�в�����ɫ�������ó����ۣ�
������H2O2��SO2����д�����߷�Ӧ�Ļ�ѧ����ʽ________________
(3)iii�е�������H2O2û�����Ա仯��������裺
�۵�1��H2O2�����ٲ�������Br-
�۵�2��B����δ��ӦH2SO3(��SO2)
Ϊ��֤�۵�2��Ӧ���е�ʵ�������������______��
(4)ͨ������ȫ��ʵ�飬�ó����ۣ�H2O2��SO2��Br2��������ǿ������˳����______��