题目内容
【题目】2017年5月5日,中国首架按照国际标准研制,拥有自主知识产权的大型客机C-919在上海浦东机场首飞,科学家在实验室研究利用催化技术将飞机尾气中的NO和CO转变成CO2和N2,其反应为2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ΔH<0。
N2(g)+2CO2(g) ΔH<0。
(1)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是____________。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
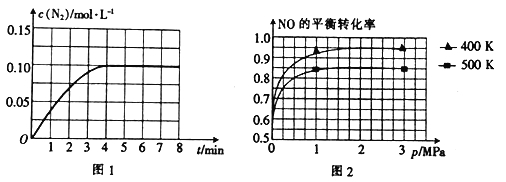
(2)若将1 molNO和2 mol CO通入2 L的恒容密闭容器中,在一定条件下发生上述反应,反应中生成的N2的物质的量浓度随时间的变化情况如图1所示。则NO从反应开始到平衡时的平均反应速率v(NO)=_________,4 min末CO的浓度为_____________ molL-1。
(3)已知上述反应中NO的平衡转化率与压强、温度的关系如图2所示。工业上催化装置比较适合的温度和压强是____________________。
【答案】 C D 0.05 molL-1·min-1 0.8 400 K,1 MPa
【解析】本题主要考查影响化学平衡的因素及其反应速率的计算。
(1)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是CD。
A.使用催化剂不改变平衡状态,不影响反应物的转化率,故A不符合题意;B.升高反应体系的温度,平衡左移,NO的转化率降低,故B不符合题意;C.该反应放热,降低反应体系的温度,平衡右移,NO的转化率提高,故C符合题意;D.该反应气体物质的量减小,加压平衡右移,NO的转化率提高,故C符合题意。故选CD。
(2)NO从反应开始到平衡时的平均反应速率v(NO)=0.20/4 molL-1·min-1=0.05 molL-1·min-1,4 min末CO的浓度(1-0.2)molL-1=0.8 molL-1。
(3)工业上催化装置比较适合的温度和压强是400 K,1 MPa。

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案【题目】在不同温度下,向V L密闭容器中加入0.5 mol NO和0.5 mol活性炭,发生反应:
2NO(g)+C(s)![]() N2(g)+CO2(g) △H= —Q kJ·mol-1(Q>0),达到平衡时的数据如下:
N2(g)+CO2(g) △H= —Q kJ·mol-1(Q>0),达到平衡时的数据如下:
温度/℃ | n (C)/mol | n(CO2)/mol |
T1 | 0.15 | |
T2 | 0.375 |
下列有关说法正确的是
A. 由上述信息可推知:T1 > T2
B. T2℃时,若反应达平衡后再缩小容器的体积,c (N2):c (NO)增大
C. T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率增大
D. T1℃时,该反应的平衡常数![]()