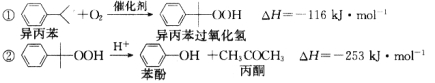
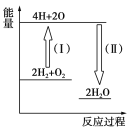
题目内容
【题目】以下是有关SO2、Cl2的性质实验。
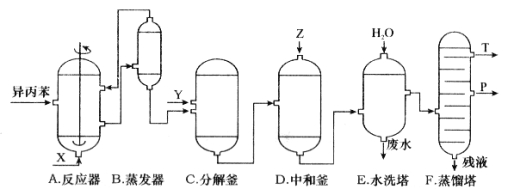
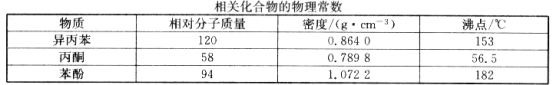
某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。
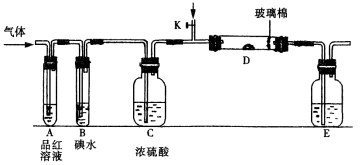
①若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同? (填“相同”或“不相同”);若D中盛铜粉,通入足量的Cl2,D中的现象是___________;若装置D中装的是五氧化二钒(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为 。
②SO2通入B中,碘水褪色,则该反应的离子方程式为 。
③E中盛有______________溶液。
某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量(填字母) ,则可以看到白色沉淀产生。
A.氨水 B.硝酸钠溶液 C.氯化钙溶液
若由元素S和O组成–2价酸根离子X,X中S和O的质量比为4∶3;当Cl2与含X的溶液完全反应后,得澄清溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式 。
【答案】
(1)①相同;Cu粉红热,并产生棕黄色烟;2SO2 + O2![]() 2SO3;
2SO3;
②SO2 + I2 + 2H2O = 4H++ 2I-+ SO42-;③NaOH;
(2)A B;(3)4Cl2 + S2O32-+ 5H2O = 2SO42-+ 8Cl-+ 10H+;
【解析】
试题分析:(1)①二氧化硫能和有色物质反应生成无色物质,所以二氧化硫有漂白性;氯气和水反应生成次氯酸,次氯酸具有强氧化性,能使有色物质褪色,所以若从左端分别通入SO2和Cl2,装置A中观察到的现象相同,都使品红褪色;铜粉在Cl2中加热Cu粉红热,并生成产生棕黄色烟氯化铜;二氧化硫和氧气在五氧化二钒作催化剂、加热条件下能发生氧化还原反应生成三氧化硫,反应方程式为 2SO2+O2 ![]() 2SO3,故答案为:相同;Cu粉红热,并产生棕黄色烟;2SO2+O2
2SO3,故答案为:相同;Cu粉红热,并产生棕黄色烟;2SO2+O2 ![]() 2SO3;
2SO3;
②SO2通入B装置碘水中,溶液颜色退去,发生了氧化还原反应:碘单质具有氧化性,二氧化硫具有还原性,被碘单质氧化为硫酸,本身被还原为碘化氢,反应的离子方程式为:SO2+I2+2H2O=4H++2I-+SO42-,故答案为:SO2+I2+2H2O=4H++2I-+SO42-;
③E为尾气处理,吸收多余的SO2和Cl2应盛有氢氧化钠溶液,故答案为:NaOH;
(2)将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量试剂仍然无法观察到沉淀产生,说明不发生反应:A、氨水加入后生成亚硫酸铵,亚硫酸根和钡离子生成沉淀,故A正确;B、硝酸钠溶液中含有硝酸根离子,通入二氧化硫后,溶液显酸性,将二氧化硫氧化成硫酸根,与钡离子生成硫酸钡沉淀,故B正确;C.氯化钙溶液和二氧化硫不反应,故C错误;故答案为:AB
(3)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4:3,所以X中S和O的原子个数比为![]() :
:![]() =3:2,所以该离子为S2O3 2-;氯气有强氧化性,能和硫代硫酸根离子发生氧化还原反应,根据题意知,该反应中有硫酸根离子生成,所以氯气中氯元素得电子生成氯离子,所以该反应的离子方程式为Cl2+S2O32-+5H2O=2SO42-+8Cl-+10H+,故答案为:4Cl2+S2O32-+5H2O=2SO42-+8Cl-+10H+。
=3:2,所以该离子为S2O3 2-;氯气有强氧化性,能和硫代硫酸根离子发生氧化还原反应,根据题意知,该反应中有硫酸根离子生成,所以氯气中氯元素得电子生成氯离子,所以该反应的离子方程式为Cl2+S2O32-+5H2O=2SO42-+8Cl-+10H+,故答案为:4Cl2+S2O32-+5H2O=2SO42-+8Cl-+10H+。

 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案【题目】(1)实验室需要450 mL 0.02 mol/L酸性KMnO4标准溶液,现有仪器:
① 托盘天平 ② 玻璃棒 ③ 药匙 ④ 200mL烧杯 ⑤ 量筒,还需要 玻璃仪器才能完成配制,需称量KMnO4固体 g。
(2)下列操作会使配制的KMnO4溶液浓度偏大的是 (填写编号,假设其他操作均正确)。
A.没有冷却至室温就转移液体到容量瓶并完成定容 |
B.使用容量瓶配制溶液,定容时,俯视刻度线 |
C.没有用蒸馏水洗涤烧杯2-3次,并将溶液移入容量瓶中 |
D.容量瓶刚用蒸馏水洗净,没有烘干就用来配制溶液 |
E.定容时,滴加蒸馏水,不慎液面略高于刻度线,吸出少量水使凹液面最低点与刻度线相切
(3)配平下面的方程式(将有关的化学计量数填入答题卡的横线上):
□KMnO4+□H2C2O4+□H2SO4——□MnSO4+□K2SO4+□H2O+□CO2↑
(4)人体血液里Ca2+的浓度一般以mg/cm3为单位。为测定血液样品中Ca2+的浓度,抽取血样20.00 mL,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用上述标准0.02 mol/L 酸性KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗13.00 mL酸性 KMnO4溶液,请计算血液样品中Ca2+的浓度为_________mg/cm3(保留到小数点后两位)。