题目内容
【题目】KNO3固体样品中含有少量的KCl、BaCl2杂质,为了提纯KNO3并分离得到BaCl2,进行如下实验操作:
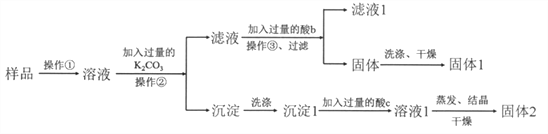
(1)试剂c的化学式是_______,固体1的化学式是________。加入过量K2CO3所发生反应的化学方程式为__________。
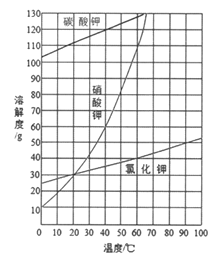
(2)结合下图各物质的溶解度曲线可知操作③的名称是______、__________。
有同学认为操作③之前无需加入过量的酸b,也能得到纯净的固体1,你认为该同学的观点是否正确?并做出相应解释_____________。
【答案】 HCl KNO3 BaCl2+K2CO3=BaCO3↓+2KCl 蒸发浓缩 冷却结晶 正确,由于硝酸钾的溶解度随温度降低急剧下降,因此有大量硝酸钾晶体析出,而碳酸钾溶解度很大,因而不会结晶析出
【解析】本题分析:本题主要考查物质的提纯方法。
(1)本实验是为了提纯KNO3并分离得到BaCl2,固体1是硝酸钾,固体2就是氯化钡,所以试剂c是稀盐酸。加入过量K2CO3,BaCl2+K2CO3=BaCO3↓+2KCl 。
(2)KNO3的溶解度随温度降低急剧下降,KCl的溶解度随温度变化较小,将KNO3和KCl分离需要蒸发浓缩、冷却结晶、趁热过滤,操作③是蒸发浓缩、冷却结晶。
正确,由于硝酸钾的溶解度随温度降低急剧下降,因此有大量硝酸钾晶体析出,而碳酸钾溶解度很大,因而不会结晶析出。

【题目】为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
![]()
![]()
(1)判断BaCl2已过量的方法是 。
(2)第④步中,相关的化学方程式是 。
(3)配制NaCl溶液时,若出现下列操作,其结果偏高还是偏低?
A.称量时NaCl已潮解( ) |
B.天平的砝码已锈蚀( ) |
C.定容摇匀时,液面下降又加水( ) |
D.定容时俯视刻度线( ) |