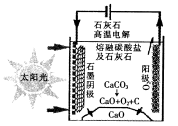
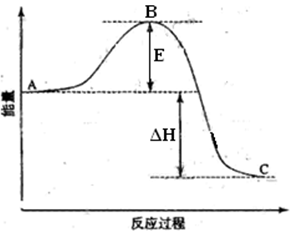
��Ŀ����
��ҵ���Ʊ�BaCl2�Ĺ�������ͼ���£�
ij�о�С����ʵ�������ؾ�ʯ����Ҫ�ɷ�BaSO4���Թ�ҵ���̽���ģ��ʵ�顣�����BaSO4(s) + 4C(s) 4CO(g) + BaS(s) ��H1���� 571.2 kJ��mol-1 ��
4CO(g) + BaS(s) ��H1���� 571.2 kJ��mol-1 ��
BaSO4(s) + 2C(s) 2CO2(g) + BaS(s) ��H2���� 226.2 kJ��mol-1 ��
2CO2(g) + BaS(s) ��H2���� 226.2 kJ��mol-1 ��
(1)�����ù���NaOH��Һ���յõ����ơ�һ��Ũ�ȵ�������Һ����������ͷų�ζ����Ϊ����������ж���һ����Ľ�������Ϊ��������� ������ţ�
A��������ˮ��Һ��ˮ��������NaOH��H2S����
B��������Һ�����տ����е�����������������NaOH��ͬʱ�����г�ζ������
C��������Һˮ��Ĺ����������տ����е�CO2���ų�H2S����
(2)��ͬ���ʵ���Ũ��BaCl2��KBr�����Һ����μ���AgNO3��Һ�������� ��������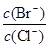 �� ʱ����ʼ���ɵڶ��ֳ���������AgNO3��Һ�Ľ�һ���μӣ���ʱ���ɵij����� Ϊ������
�� ʱ����ʼ���ɵڶ��ֳ���������AgNO3��Һ�Ľ�һ���μӣ���ʱ���ɵij����� Ϊ������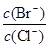 �� ������С��ʼ�ղ��䣩��[��֪Ksp(AgBr)��5.4��10-13��Ksp(AgCl)��2.0��10-10]
�� ������С��ʼ�ղ��䣩��[��֪Ksp(AgBr)��5.4��10-13��Ksp(AgCl)��2.0��10-10]
(3)��ӦC(s) + CO2(g) 2CO(g)�ġ�H�� kJ��mol-1��
2CO(g)�ġ�H�� kJ��mol-1��
(4)ʵ�������б�����������̿��ͬʱ��Ҫͨ���������Ŀ���� ��
��1��C��2�֣���2��AgBr 2.7��10-3 AgCl ʼ�ղ��䣨��1�֣���3��+172.5 ��2�֣�
��4��ʹ���ᱵ��ֱ���ԭ����������IJ������� �٢�Ϊ���ȷ�Ӧ��̿��������Ӧά�ַ�Ӧ������¡���2�֣���(��10��)
���������������1��A�����������ӵ�ˮ��̶�һ���Ǻ����ģ����������ˮ��Һ��ˮ�����ɵ�H2S���岻���������A����ȷ��B�������Ӽ��黹ԭ�ԣ����������Һ���տ����е�����������������NaOH��ͬʱ���ɵ���S���ò���H2S���壬B����ȷ��C��������Һˮ��Ĺ����������տ����е�CO2���ų�H2S���壬�Ӷ��ͷų���ζ�����壬C��ȷ����ѡC��
��2�������廯�����ܶȻ�����С���Ȼ������ܶȻ������������ͬ���ʵ���Ũ��BaCl2��KBr�����Һ����μ���AgNO3��Һ���������廯���������������Ȼ�������ʱ����Һ��һ��ͬʱ����c(Ag��)��c(Cl��)��Ksp(AgCl)��2.0��10-10��c(Ag��)��c(Br��)��Ksp(AgBr)��5.4��10-13��������Һ��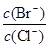 ��
��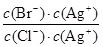 ��
��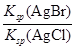 ��2.7��10-3������AgNO3��Һ�Ľ�һ���μӣ���ʱ���ɵij������Ȼ�������Ϊ����������Һ�¶Ȳ��䣬�ܶȻ��������䣬����
��2.7��10-3������AgNO3��Һ�Ľ�һ���μӣ���ʱ���ɵij������Ȼ�������Ϊ����������Һ�¶Ȳ��䣬�ܶȻ��������䣬����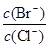 ���䡣
���䡣
��3����֪��ӦBaSO4(s) + 4C(s) 4CO(g) + BaS(s) ��H1���� 571.2 kJ��mol-1 �٣�
4CO(g) + BaS(s) ��H1���� 571.2 kJ��mol-1 �٣�
BaSO4(s) + 2C(s) 2CO2(g) + BaS(s) ��H2���� 226.2 kJ��mol-1 �ڣ�����ݸ�˹���ɿ�֪���٣��ڣ���2���õ���ӦC(s) + CO2(g)
2CO2(g) + BaS(s) ��H2���� 226.2 kJ��mol-1 �ڣ�����ݸ�˹���ɿ�֪���٣��ڣ���2���õ���ӦC(s) + CO2(g) 2CO(g)�����Ը÷�Ӧ�ġ�H����(571.2 kJ��mol-1��226.2 kJ��mol-1)��2����172.5kJ��mol-1��
2CO(g)�����Ը÷�Ӧ�ġ�H����(571.2 kJ��mol-1��226.2 kJ��mol-1)��2����172.5kJ��mol-1��
��4��������̼��ʹ���ᱵ��ֱ���ԭ����������IJ�����������٢�Ϊ���ȷ�Ӧ��̿��������Ӧ���ȣ�����ά�ַ�Ӧ������¡�
���㣺�������Ƶ����ʡ��ܶȻ��������㡢��Ӧ�ȵļ����Լ���������Է�Ӧ��Ӱ��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�ʵʩ�Լ�����Դ�˷Ѻͽ��ͷ����ŷ�Ϊ�������ݵĽ��ܼ������ߣ���Ӧ��ȫ���������⡢������Դ��Լ�͡������Ѻ������ı�Ȼѡ������ҵ�ķ�չ������Ϲ��ҽ��ܼ��ŵ�����Ҫ����������֪ʶ����������������ѧ֪ʶ������������⣺
��1����֪ij��Ӧ��ƽ�����ʽΪ�� ������Ӧ�Ļ�ѧ��ӦΪ��_____________________________
������Ӧ�Ļ�ѧ��ӦΪ��_____________________________
��2������ˮú���ϳɶ����ѵ�������Ӧ���£�
��2H2��g��+CO��g�� CH3OH��g������H=��90.8 kJ/mol
CH3OH��g������H=��90.8 kJ/mol
��2CH3OH��g�� CH3OCH3��g��+H2O��g������H=��23.5 kJ/mol
CH3OCH3��g��+H2O��g������H=��23.5 kJ/mol
��CO��g��+ H2O��g�� CO2��g��+H2��g������H=��41.3 kJ/mol
CO2��g��+H2��g������H=��41.3 kJ/mol
�ܷ�Ӧ��3H2��g��+3CO��g�� CH3OCH3��g��+CO2��g���Ħ�H="__________" ��
CH3OCH3��g��+CO2��g���Ħ�H="__________" ��
�����ѣ�CH3OCH3��ֱ����ȼ�ϵ�ؾ��������죬Ч�ʸߵ��ŵ㣬�������Ϊ���ԣ��õ�صĸ�����ӦΪ_____________________________��
��3��ú����ͨ��ͨ���о���ͬ�¶���ƽ�ⳣ���Խ������ʵ�����⡣��֪�������һ����̼��ˮ�������뷴Ӧ��ʱ���ᷢ�����·�Ӧ��CO��g��+H2O��g�� H2��g��+CO2��g�����÷�Ӧƽ�ⳣ�����¶ȵı仯���±���ʾ��
H2��g��+CO2��g�����÷�Ӧƽ�ⳣ�����¶ȵı仯���±���ʾ��
| �¶�/�� | 400 | 500 | 800 |
| ƽ�ⳣ��K | 9.94 | 9 | 1 |
�÷�Ӧ������Ӧ������_________��Ӧ������ȡ����ȡ���������500��ʱ���У�����ʼʱCO��H2O����ʼŨ�Ⱦ�Ϊ0.020mol/L���ڸ������£�CO��ƽ��ת����Ϊ��________��
��4���Ӱ����������������ᣬ�˹������漰���������NO��NO2��N2O4�ȡ��Է�Ӧ N2O4��g��
 2NO2��g�� ��H>0�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ����___________��
2NO2��g�� ��H>0�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ����___________��
A��A��C����ķ�Ӧ���ʣ�A��C
B��A��C�����������ɫ��A�Cdz
C��B��C����������ƽ����Է���������B��C
D����״̬B��״̬A�������ü��ȵķ���
E��A��C����Ļ�ѧƽ�ⳣ����A��C
��5��NO2���ð�ˮ��������NH4NO3��25��ʱ����m mol NH4NO3����ˮ����Һ�����ԣ������Һ�μ�n L��ˮ����Һ�����ԣ���μӰ�ˮ�Ĺ�����ˮ�ĵ���ƽ�⽫______������������������ƶ������μӰ�ˮ��Ũ��Ϊ_______mol��L-1����NH3��H2O�ĵ���ƽ�ⳣ��ȡKb=2X10-5 mol��L-1��
��6��ij���е�λ����ԭ���ԭ������SO2��O2���Ʊ����ᣬװ������ͼ���缫Ϊ��IJ������������壬ͬʱҲ��ʹ������������Һ��ֽӴ���

����Һ��H+���ƶ�������______ ����______��������A��B��ʾ��
��B�缫�ĵ缫��ӦʽΪ__________________________��
�ҹ��Ǹ��������,��������Ϊ�����һ,��¯��������Ϊ�ձ������������
I.��֪��Ӧ 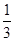 Fe2O3(s)+ CO(g)
Fe2O3(s)+ CO(g)
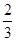 Fe(s)+ CO2(g) ��H��-23.5 kJ��mol-1���÷�Ӧ��
Fe(s)+ CO2(g) ��H��-23.5 kJ��mol-1���÷�Ӧ��
1000���ƽ�ⳣ������4����һ���ݻ�Ϊ10L���ܱ�������,1000��ʱ����Fe��Fe2O3��CO��CO2��1. 0mol,��Ӧ����l0min��ﵽƽ�⡣
��1��CO��ƽ��ת����=____________
��2�������CO��ƽ��ת����,�ٽ�Fe2O3��ת��,�ɲ�ȡ�Ĵ�ʩ��________
a����߷�Ӧ�¶�
b������Ӧ��ϵ��ѹǿ
c��ѡȡ���ʵĴ���
d����ʱ���ջ��Ƴ�����CO2
e�������ʯ,ʹ����ƽ���������ֽӴ�
��.��¯���������ķ����е�CO�ɽ��л���,ʹ����һ�������º�H2��Ӧ�Ʊ��״�:
CO(g)+ 2H2(g) CH3OH(g)�������ͼʾ�ش���������:
CH3OH(g)�������ͼʾ�ش���������: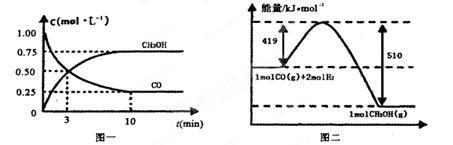
��1���ӷ�Ӧ��ʼ��ƽ��,��H2Ũ�ȱ仯��ʾƽ����Ӧ����v(H2)=________
��2�������¶Ⱥ�������ͬ�������ܱ�������,����ͬ��ʽͶ�뷴Ӧ��,��÷�Ӧ�ﵽƽ�ⅼ���й��������±���
| ���� | ��Ӧ��Ͷ����� | ��Ӧ��� ת���� | CH3OH��Ũ�� | �����仯 (Q1��Q2��Q3������0) |
| �� | 1mol CO��2mol H2 | ��1 | c1 | �ų�Q1kJ���� |
| �� | 1mol CH3OH | ��2 | c2 | ����Q2kJ���� |
| �� | 2mol CO��4mol H2 | ��3 | c3 | �ų�Q3kJ���� |
�����й�ϵ��ȷ����________
A��c1=c2 B��2Q1=Q3 C��2��1=��3 D����1+��2 =1
E���÷�Ӧ������1mol CH3OH����ų�(Q1+Q2)kJ����
���Լ���Ϊȼ�ϵ����͵�أ���ɱ�����������Ϊȼ�ϵĴ�ͳȼ�ϵ�أ�Ŀǰ�õ��㷺���о�����ͼ��Ŀǰ�о��϶��һ�����������ȼ�ϵ�ع���ԭ��ʾ��ͼ���ش��������⣺
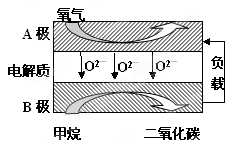
��1��B���ϵĵ缫��ӦʽΪ
��2�����ø�ȼ�ϵ������Դ����ʯī���缫���100mL 1mol/L������ͭ��Һ���������ռ���������������ʱ�����������ĵļ�������Ϊ ������£���
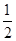 O2(g)=FeO(s)����H����272.0 kJ��mol��1
O2(g)=FeO(s)����H����272.0 kJ��mol��1 O2(g)=Al2O3(s)����H����1675.7 kJ��mol��1
O2(g)=Al2O3(s)����H����1675.7 kJ��mol��1
 Na2S(s)��4H2O(g)
Na2S(s)��4H2O(g)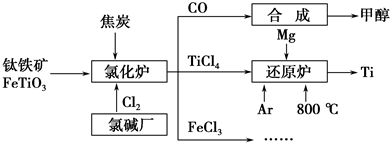
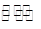 C H4 (g)+2 H2O(g)����һ�ݻ�Ϊ2 L�ĺ����ܱ������г���һ������CO2��H2����300��ʱ����������Ӧ���ﵽƽ��ʱ�����ʵ�Ũ�ȷֱ�ΪCO2 0.2 mol��Lһ1��H2 0.8 mol��Lһ1��CH40.8 mol��Lһ1��H2O1.6 mol��Lһ1����CO2��ƽ��ת����Ϊ________��300 ��ʱ������Ӧ��ƽ�ⳣ��K=____________________��200��ʱ�÷�Ӧ��ƽ�ⳣ��K=64.8����÷�Ӧ�ġ�H_____(���������<��)O��
C H4 (g)+2 H2O(g)����һ�ݻ�Ϊ2 L�ĺ����ܱ������г���һ������CO2��H2����300��ʱ����������Ӧ���ﵽƽ��ʱ�����ʵ�Ũ�ȷֱ�ΪCO2 0.2 mol��Lһ1��H2 0.8 mol��Lһ1��CH40.8 mol��Lһ1��H2O1.6 mol��Lһ1����CO2��ƽ��ת����Ϊ________��300 ��ʱ������Ӧ��ƽ�ⳣ��K=____________________��200��ʱ�÷�Ӧ��ƽ�ⳣ��K=64.8����÷�Ӧ�ġ�H_____(���������<��)O��