题目内容
以下事实不能用勒夏特列原理解释的是( )
| A.增大压强,有利于二氧化硫和氧气反应生成三氧化硫 |
| B.工业制取硫酸和合成氨反应都要使用催化剂 |
| C.合成氨工业生产中,把合成塔中的氨气不断抽出 |
| D.实验室常用排饱和食盐水的方法收集氯气 |
B
试题分析:二氧化硫催化氧化生成三氧化硫的反应是气体体积缩小的反应,增大压强,平衡向生成三氧化硫的方向移动,A正确;催化剂同等程度改变正、逆反应速率,对平衡移动无影响,B不能用勒沙特列原理解释;合成氨反应中,把氨移出,减少生成物浓度,平衡向右移动,C正确;氯气溶于水的反应(Cl2+H2O
 H++Cl-+HClO)是可逆反应,饱和食盐水中氯离子浓度大,增大氯离子浓度,平衡向左移动,D正确。
H++Cl-+HClO)是可逆反应,饱和食盐水中氯离子浓度大,增大氯离子浓度,平衡向左移动,D正确。点评:催化剂同等程度改变正、逆反应速率,对平衡移动无影响。

练习册系列答案
相关题目
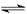 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据: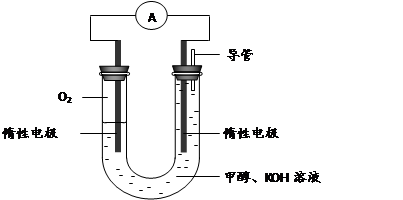
 N2O4(g) ΔH<0。现将NO2和N2O4 混合气体通入恒温密闭容器中,反应中物质浓度随时间的变化如图。下列说法正确的是
N2O4(g) ΔH<0。现将NO2和N2O4 混合气体通入恒温密闭容器中,反应中物质浓度随时间的变化如图。下列说法正确的是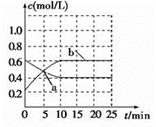
 NaCl(l)+ K(g)选取适宜的温度,使K成蒸汽从反应混合物中分离出来
NaCl(l)+ K(g)选取适宜的温度,使K成蒸汽从反应混合物中分离出来 C(s) + D(g);(正反应吸热)。下图所示为正逆反应速率(v)与时间(t)关系的示意图,如果在t1时刻改变以下条件:( )
C(s) + D(g);(正反应吸热)。下图所示为正逆反应速率(v)与时间(t)关系的示意图,如果在t1时刻改变以下条件:( )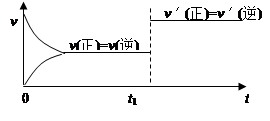
 2XY3(g) ΔH=-92.6 kJ·mol-1实验测得反应在起始、达到平衡时的有关数据如下表所示:下列叙述不正确的是
2XY3(g) ΔH=-92.6 kJ·mol-1实验测得反应在起始、达到平衡时的有关数据如下表所示:下列叙述不正确的是 2C(g)(正反应放热)中,为了增大A的转化率,应采用的反应条件是( )
2C(g)(正反应放热)中,为了增大A的转化率,应采用的反应条件是( ) N2O4 ΔH<0,若把烧瓶置于100℃的沸水中,下列情况:①颜色②平均摩尔质量③质量④压强⑤密度中不变的是
N2O4 ΔH<0,若把烧瓶置于100℃的沸水中,下列情况:①颜色②平均摩尔质量③质量④压强⑤密度中不变的是