题目内容
9.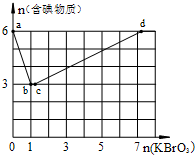 现向含6mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示.
现向含6mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示.已知①BrO3-+6I-+6H+═3I2+Br-+3H2O;②2BrO3-+I2═2IO3-+Br2;
请回答下列问题:
(1)由反应②有同学由此得出氧化性:I2>Br2的结论,你认为是否正确否(填是或否),并说明理由该反应中I2作还原剂,Br2为还原产物,应得出还原性I2>Br2结论.
(2)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为1:6,还原产物是KBr.
(3)b→c过程中只有一种元素的化合价发生变化,写出该过程的离子反应方程式BrO3-+5Br-+6H+=3Br2+3H2O.
(4)含6mol KI的硫酸溶液所能消耗n(KBrO3)的最大值为7.2mol.
(5)n(KBrO3)=4时,对应含碘物质的化学式为I2,KIO3.
分析 (1)根据反应2BrO3-+I2═2IO3-+Br2,氧化剂的氧化性强于氧化产物的氧化性来回答;
(2)b点时,KI反应完全,有图象可知参加反应的KI为6mol,KBrO3为1mol,结合氧化剂、还原剂得失电子数目相等判断还原产物;
(3)b→c过程中,仅有一种元素发生化合价变化,应是BrO3-与Br-之间的氧化还原反应;
(4)根据关系式KI~I2~IO3-以及bc段反应BrO3-~Br-,写出反应的总方程式进行计算;
(5)n(KBrO3)=4时,发生的反应依次有6H++6I-+BrO3-=Br-+3I2+3H2O,BrO3-+5Br-+6H+=3Br2+3H2O,2BrO3-+I2=2IO3-+Br2,据此计算.
解答 解:(1)根据反应:2BrO3-+I2═2IO3-+Br2,还原剂的还原性强于还原产物的氧化性,所以得出还原性I2>Br2,故答案为:否;该反应中I2作还原剂,Br2为还原产物,应得出还原性I2>Br2结论;
(2)b点时,KI反应完全,有图象可知参加反应的KI为6mol,KBrO3为1mol,则消耗的氧化剂与还原剂物质的量之比为1:6,
发生反应为6I-+BrO3-=Br-+3I2,还原产物是KBr,
故答案为:1:6;KBr;
(3)b→c过程中,仅有一种元素发生化合价变化,应是BrO3-与Br-之间的氧化还原反应,反应的离子方程式为BrO3-+5Br-+6H+=3Br2+3H2O,
故答案为:BrO3-+5Br-+6H+=3Br2+3H2O;
(4)发生的反应依次有6I-+6H++BrO3-=Br-+3I2+3H2O,BrO3-+5Br-+6H+=3Br2+3H2O,2BrO3-+I2=2IO3-+Br2,
总反应为5I-+6H++6BrO3-=5IO3-+3Br2+3H2O,则含6molKI的硫酸溶液所能消耗n(KBrO3)的最大值为1.2×6mol=7.2mol,
故答案为:7.2;
(5)n(KBrO3)=4时,发生的反应依次有6I-+BrO3-=Br-+3I2,BrO3-+5Br-+6H+=3Br2+3H2O,2BrO3-+I2=2IO3-+Br2,6molKI生成I2,需要1molKBrO3,同时生成1molKBr,发生BrO3-+5Br-+6H+=3Br2+3H2O,需要0.2molKBrO3,如I2完全被氧化生成KIO3,还应需要6molKBrO3,
则n(KBrO3)=4时,对应含碘物质的化学式为I2,KIO3,
故答案为:I2,KIO3.
点评 本题考查氧化还原反应,题目难度中等,本题注意根据关系的关系式计算,为解答该题的关键,也是易错点.

| A | NaCl═Na++Cl NH3•H2O?NH4++OH- | 均属于电离方程式 |
| B | 向溶液中滴加盐酸酸化过的BaCl2溶液,出现白色沉淀 | 说明该溶液中一定有SO${\;}_{4}^{2-}$ |
| C | Ba2++SO${\;}_{4}^{2-}$═BaSO4↓; HCO${\;}_{3}^{-}$+OH-═CO${\;}_{3}^{2-}$+H2O | 均可表示一类反应 |
| D | Cl2+2NaOH═NaCl+NaClO+H2O; 3S+6NaOH═2Na2SO3+3H2O | Cl2和S在反应中既作氧化剂又作还原剂 |
| A. | A | B. | B | C. | C | D. | D |
| 实验序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)实验1,反应在10至20分钟时间内A平均速率为0.013mol/(L.min).
(2)实验2,A的初始浓度c2=1.0 mol•L-1,推测实验2中还隐含的条件是加入催化剂.
(3)800℃时该反应的平衡常数K=0.25
(4)设实验3的反应速率为v3,实验1的反应速率为v1,则v3>v1(填>、<、=),且C3=1.2mol•L-1.
| A. | 2mol/L Ba(OH)2溶液中Ba2+的物质的量和OH-的物质的量 | |
| B. | 200mL 1mol/L氯化钙溶液中c(Cl-)和100 mL 2mol/L氯化钾溶液中c(Cl-) | |
| C. | 20%NaOH溶液中NaOH的物质的量浓度和10%NaOH溶液中NaOH的物质的量浓度 | |
| D. | 64g二氧化硫中氧原子数和标准状况下22.4L一氧化碳中氧原子数 |
| A. | 1.0 L 1.0 mo1•L-1的NaAlO2水溶液中含有的氧原子数为2NA | |
| B. | 56 g铁片投入足量浓H2SO4中生成NA个SO2分子 | |
| C. | 标准状况下,22.4 L氨水含有NA个NH3分子 | |
| D. | 常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA |
| A. | 铜用于制造导线 | B. | 干冰用于人工降雨 | ||
| C. | 天然气用作燃料 | D. | 石墨棒作干电池电极 |
| A. | 用土填埋废弃塑料,防止白色污染 | |
| B. | 使用车乙醇汽油,防止温室效应 | |
| C. | 化工厂加高烟囱排放废气,防止酸雨 | |
| D. | 废旧电池中汞的回收可减少对环境的污染 |
| A. | 3个 | B. | 4个 | C. | 5个 | D. | 6个 |
第一份加入AgNO3溶液有沉淀产生;
第二份加足量NaOH溶液加热后,收集到0.03mol气体;
第三份加足量BaCl2溶液后,得到干燥沉淀4.30g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g
综合上述实验,你认为以下结论正确的是( )
| A. | 该混合液中一定含有:K+、NH4+、CO32-、SO42-,可能含Cl- | |
| B. | 该混合液中-定含有:NH4+、CO32-、SO42-,可能含K+、Cl- | |
| C. | 该混合液中一定含有:NH4+、CO32-、SO42-、Cl-,可能含K+ | |
| D. | 该混合液中:c(K+)≥0.1mol/L c(CO32-)=0.1mol/L |