题目内容
16.利用所学的有关知识设计以下有机合成路线,并说明在合成中你是通过怎样的反应完成官能团转化或碳链增长的(除指定的起始物外,其他试剂可自行选用).(1)从1-溴丙烷制取2-丙醇;
(2)由溴乙烷合成1-丁炔.
分析 (1)先根据卤代烃在氢氧化钠醇溶液、加热条件下发生消去反应生成烯烃,再利用烯烃与溴化氢发生加成反应得到2-溴丙烷,2-溴丙烷在碱性条件下水解生成2-丙醇;
(2)先根据卤代烃在氢氧化钠醇溶液、加热条件下发生消去反应生成烯烃,再利用烯烃与卤素单质发生加成反应得到1,2-二溴乙烷,1,2-二溴乙烷在氢氧化钠醇溶液、加热条件下发生消去反应即可得到产物来书写方程式.
解答 解:(1)CH3CH2CH2Br在氢氧化钠醇溶液、加热条件下发生消去反应:CH3CH2CH2Br+NaOH$→_{△}^{醇}$CH3CH═CH2↑+NaBr+H2O,CH3CH═CH2与溴化氢发生加成反应CH3CH═CH2+HBr-→CH3CHBrCH3在氢氧化钠水溶液、加热条件下发生水解反应:CH3CHBrCH3+NaOH$\stackrel{△}{→}$CH3CH(OH)CH3+NaBr,
答:CH3CH2CH2Br+NaOH$→_{△}^{醇}$CH3CH═CH2↑+NaBr+H2O,CH3CH═CH2+HBr-→CH3CHBrCH3,CH3CHBrCH3+NaOH$\stackrel{△}{→}$CH3CH(OH)CH3+NaBr;
(2)CH3CH2Br在氢氧化钠醇溶液、加热条件下发生消去反应:C2H5Br+NaOH$→_{△}^{醇}$CH2═CH2↑+NaBr+H2O,CH2═CH2与溴水发生加成反应:CH2═CH2+Br2-→CH2BrCH2Br,
CH2BrCH2Br在氢氧化钠醇溶液、加热条件下发生消去反应:CH2BrCH2Br+2NaOH$→_{△}^{醇}$CH≡CH↑+2NaBr,
答:C2H5Br+NaOH$→_{△}^{醇}$CH2═CH2↑+NaBr+H2O,CH2═CH2+Br2-→CH2BrCH2Br,CH2BrCH2Br+2NaOH$→_{△}^{醇}$CH≡CH↑+2NaBr.
点评 本题结合有机物的结构和性质考查了有机物的合成,明确常见的反应类型、物质结构与性质的关系、掌握官能团的性质是解题的关键,题目难度中等.

 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案| A. | 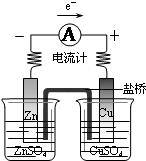 探究原电池原理 探究原电池原理 | B. |  制备无水氯化铁 | C. | 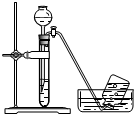 探究铁与水反应 探究铁与水反应 | D. |  收集氨气 收集氨气 |
| A. | 乙烯的结构简式:CH2CH2 | |
| B. | 碳正离子 中质子数与电子数之比值为3:2 中质子数与电子数之比值为3:2 | |
| C. | 水合氢离子的结构式为 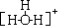 | |
| D. | NaHCO3水解反应的离子方程式:HCO3-+H2O?H3O++CO32- |
| A. | C2H6 | B. | C3H8 | C. | C4H10 | D. | C5H12 |
| A. | 55kJ | B. | 220kJ | C. | 550kJ | D. | 1108kJ |
