题目内容
1.化学用语是学习化学的重要工具.以下化学用语或表述正确的是( )| A. | 乙烯的结构简式:CH2CH2 | |
| B. | 碳正离子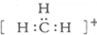 中质子数与电子数之比值为3:2 中质子数与电子数之比值为3:2 | |
| C. | 水合氢离子的结构式为  | |
| D. | NaHCO3水解反应的离子方程式:HCO3-+H2O?H3O++CO32- |
分析 A.结构简式不能省略官能团碳碳双键;
B.质子数为6+3=9,电子数为9-1=8;
C.水合氢离子为阳离子,含3个O-H共价键;
D.水解生成碳酸、NaOH.
解答 解:A.乙烯分子中含有碳碳双键,乙烯的结构简式为CH2=CH2,故A错误;
B.碳正离子的质子数为9,核外电子数为8,质子数与电子数之比值为9:8,故B错误;
C.水合氢离子为阳离子,含3个O-H共价键,水合氢离子的结构式为  ,故C正确;
,故C正确;
D.碳酸氢钠水解反应的离子方程式为HCO3-+H2O?OH-+H2CO3,故D错误;
故选C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重水解离子反应及常见化学用语的考查,题目难度中等.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
11.根据原子结构及元素周期律的知识,下列推断正确的是( )
| A. | H、D、T三种氢的核素在周期表中的位置不同 | |
| B. | 元素简单气态氢化物越稳定,则非金属性越强 | |
| C. | 核外电子层结构相同的离子,核电荷数越大其离子半径也越大 | |
| D. | ⅠA与ⅦA元素形成的化合物都是离子化合物 |
12.某课外实验小组设计的下列实验合理的是( )
| A. | 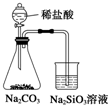 比较非金属性强弱Cl>C>Si | B. | 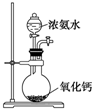 制备少量氨气 | ||
| C. | 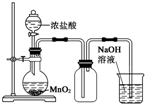 实验室制氯气 | D. | 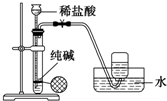 实验室制二氧化碳 |
6.下表列出了短周期内除稀有气体外的四种元素W、X、Y、Z的有关信息.请回答下列问题:
(1)写出下列元素的元素符号:XO,ZS.
(2)X、Z的最简单氢化物是由共价(填“离子”或“共价”)键形成的物质,其中稳定性较弱的氢化物的化学式为H2S.
(3)化合物YXW是由离子键和共价键构成的离子化合物(填“离子”或“共价”)
(4)由W、X、Y、Z四种元素组成的常见化合物的化学式为NaHSO4、NaHSO3,写出这两种物质发生反应的离子方程式:H++HSO3-=SO2↑+H2O.
| 原子序数 | 元素 | 有关信息 |
 | W | 质子数与Y的最外层电子数相等 |
| X | 最低化合价为-2 | |
| Y | 四种元素种仅有的金属元素 | |
| Z | 与Y的原子序数之和为W、X原子序数之和的3倍 |
(2)X、Z的最简单氢化物是由共价(填“离子”或“共价”)键形成的物质,其中稳定性较弱的氢化物的化学式为H2S.
(3)化合物YXW是由离子键和共价键构成的离子化合物(填“离子”或“共价”)
(4)由W、X、Y、Z四种元素组成的常见化合物的化学式为NaHSO4、NaHSO3,写出这两种物质发生反应的离子方程式:H++HSO3-=SO2↑+H2O.
13.下列叙述错误的是( )
| A. | 向蛋白质溶液中加入CuSO4溶液,蛋白质发生变性 | |
| B. | 一定条件下,乙醇能被氧化成一种刺激性气味的液体 | |
| C. | 用Cl2和NaOH溶液为原料制备次氯酸钠 | |
| D. | 海水提溴和生产玻璃过程中均涉及氧化还原反应 |
10.2L N2和CH4的混合气体与4L O2点燃充分反应后,用干燥剂除去水分,剩余气体的体积5L.原来气体中N2和CH4的物质的量之比(各气体体积都在相同的温度、压强下测定)为 ( )
| A. | 1:3 | B. | 1:1 | C. | 2:1 | D. | 3:1 |
11.下列指定微粒的数目相等的是( )
| A. | 等物质的量的水与重水含有的中子数 | |
| B. | 等质量的乙烯和丙烯中含有的共有电子对数 | |
| C. | 同温、同压、同体积的CO和NO含有的质子数 | |
| D. | 等物质的量的铁和铝分别与足量氯气完全反应时转移的电子数 |