题目内容
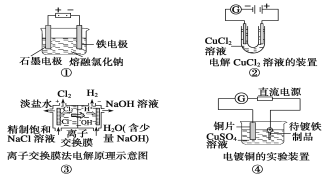
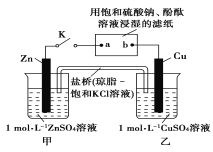
【题目】将如图所示实验装置的K闭合,下列判断不正确的是( )
A.Cu电极上发生还原反应
B.片刻后甲池中c(SO42-)不变
C.电子沿Zn→a→b→Cu路径流动
D.片刻后可观察到滤纸a点变红
【答案】C
【解析】
甲、乙装置能自发的进行氧化还原反应,所以是原电池,锌易失电子作负极,铜作正极,则含有硫酸钠溶液的滤纸是电解池,a是阴极,b是阳极,阴极上氢离子放电,阳极上氢氧根离子放电,电子从负极沿导线流向电解池阴极,原电池放电时,阴离子向负极移动,阳离子向正极移动。
甲、乙装置能自发的进行氧化还原反应,所以是原电池,锌易失电子作负极,铜作正极,则含有硫酸钠溶液的滤纸是电解池,a是阴极,b是阳极。
A、铜电极上铜离子得电子发生还原反应而生成铜,选项A正确;
B、硫酸根离子浓度基本保持不变,选项B正确;
C、电子流向是负极到正极,但a→b这一环节是在溶液中导电,是离子导电,电子并没沿此路径流动,选项C不正确;
D、滤纸a点是阴极,氢离子放电,水电离平衡破坏,附近氢氧根离子浓度增大,酚酞变红,选项D正确;
答案选C。

 导学全程练创优训练系列答案
导学全程练创优训练系列答案【题目】废旧印刷电路板中铜元素含量较高,为充分利用资源,变废为宝实验小组探究利用废旧印刷电路板来制备胆矾,具体流程如图所示:
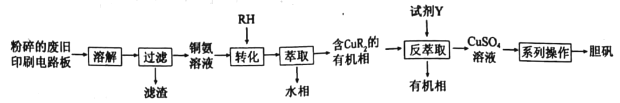
请回答:
(1)“溶解”过程中,为选择合适的溶解试剂,查阅资料后,小组同学设计如下实验。
实验编号 | 铜片质量/g | 试剂及用量 | 现象 |
1号 | 0.5 | 30%H2O250mL、蒸馏水8mL | 10h后,溶液变为浅蓝色,铜片表面附着蓝色沉淀 |
2号 | 0.5 | 30%H2O250mL、5mol·L-1H2SO48mL | 开始铜片表面有气泡生成(先慢后快,40min后,溶液蓝色明显铜片表面光亮 |
3号 | 0.5 | 30%H2O250mL、5mol·L-1氨水8mL | 立即产生大量气泡溶液为深蓝色,铜片表面附着少量蓝色沉淀 |
注:深蓝色溶液为铜氨溶液。
①1号实验中发生反应的化学方程式为______________。
②实验室检验2号实验中产生气体的操作和现象为______________。
③与2号实验相比,3号实验的优点是生成了铜氨配合物,加快了反应速率;其不足之处为______________。
④为弥补3号实验的不足,该小组继续进行改进,设计了4号实验(见下表,并得到了预期的实验现象。
实验编号 | 铜片质量/g | 试剂及用量 | 现象 |
4号 | 0.5 | 30%H2O250mL5mol·L-1氨水8mL和适量试剂X | 立即产生大量气泡,溶液为深蓝色,铜片表面仍光亮 |
则4号实验中,试剂x应为______________。
(2)“转化”时铜氨溶液中的Cu(NH3)42+与有机物RH发生反应的离子方程式为______________。“反萃取”过程中,所加试剂Y的化学式为______________。
(3)“系列操作”具体指_____________(填选项字母)。
A.蒸发浓缩、趁热过滤、洗涤、干燥
B.蒸发浓缩至溶液表面出现晶膜后停止加热,冷却、过滤、洗涤、干燥
C.蒸发浓缩至大量晶体析出后停止加热,冷却、过滤、洗涤、干燥
(4)为测定铜氨溶液中铜元素的含量,可采用如下方法:
i.移取500mL铜氨溶液于锥形瓶中,滴加稀H2SO4,调节溶液的pH为3-4
ⅱ.加入适当过量的KI溶液,并加入3mL0.5%淀粉溶液(![]() );
);
ⅲ.用0.1000mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准液体积为5.80mL(I2+2S2O32-=2I-+S4O262-)。
①iii中滴定至终点时,溶液的颜色变化为______________。
②该铜氨溶液中铜元素的含量为______________g·mL-1(保留两位有效数字)。