题目内容
已知W、X、Y、Z为短周期元素,它们的原子半径依次增大,W与Z、X和Y分别同主族,Y、Z同周期。Z能与X形成两种常见的离子化合物,离子个数比均为2:1。下列说法错误的是
| A.Y、Z、X、W的原子序数依次减小 |
| B.W与X可形成既含极性共价键又含非极性共价键的化合物 |
| C.由W、X、Y、Z四种元素组成的常见化合物一定显酸性 |
| D.X的简单氢化物的沸点低于Y的简单氢化物的沸点 |
D
试题分析:Z能与X形成两种常见的离子化合物,离子个数比均为2:1,在短周期元素中应该是Na和O。X的原子半径小于Z的,则X是O,Z是Na。W与Z、X和Y分别同主族,Y、Z同周期,所以Y是S,W的原子半径最小,因此W是H。
A、S、Na、O、H的原子序数依次减小,A正确;
B、H和O生成的H2O2中既含极性共价键又含非极性共价键,B正确;
C、由四种元素形成的化合物是NaHSO4或NaHSO3,其溶液均显酸性,C正确;
D、水分子间存在氢键,所以H2O的沸点高于H2S的沸点,D不正确,答案选D。

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
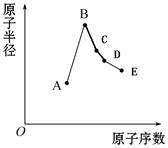


 位于大立方体顶点和面心,
位于大立方体顶点和面心,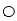 位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处▽所代表的微粒是 (填具体的微粒符号)
位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处▽所代表的微粒是 (填具体的微粒符号)