题目内容
W、X、Y、Z为四种短周期主族元素,其位置关系如图。

(1)若X原子的最外层电子数是次外层的3倍。
①元素X在周期表中的位置___________________________________。
②工业上由W的单质制备W的气态氢化物的化学方程式是
_______________________________________________________________________。
(2)若四种元素中只有一种金属元素。
①冶炼Y的化学方程式是__________________________________________。
②工业上,将X的单质与Z的最高价氧化物加热到1900℃以上可制得一种新型陶瓷(ZX),同时得到一种可燃性气体,该反应的化学方程式是
_________________________________
③为比较X、Z最高价氧化物的水化物酸性强弱,某同学设计如下实验。

I. B试管中盛放的试剂是______________________。
II. C试管中反应的化学方程式是___________________________________。

(1)若X原子的最外层电子数是次外层的3倍。
①元素X在周期表中的位置___________________________________。
②工业上由W的单质制备W的气态氢化物的化学方程式是
_______________________________________________________________________。
(2)若四种元素中只有一种金属元素。
①冶炼Y的化学方程式是__________________________________________。
②工业上,将X的单质与Z的最高价氧化物加热到1900℃以上可制得一种新型陶瓷(ZX),同时得到一种可燃性气体,该反应的化学方程式是
_________________________________
③为比较X、Z最高价氧化物的水化物酸性强弱,某同学设计如下实验。

I. B试管中盛放的试剂是______________________。
II. C试管中反应的化学方程式是___________________________________。
(12分,每空2分)(1)① 第2周期VIA族②N2+3H2高温、高压催化剂 2NH3
(2)①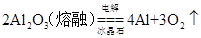 ②
②
③I. 饱和NaHCO3溶液(答NaHCO3给分) II.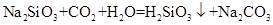
(2)①
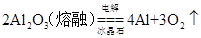 ②
②
③I. 饱和NaHCO3溶液(答NaHCO3给分) II.
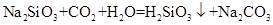
试题分析:(1)若X原子的最外层电子数是次外层的3倍,X是第二周期元素,所以X是氧元素,则W是氮元素,Y是P元素,Z是S元素。
①元素X在周期表中的位置第2周期VIA族。
②工业上由W的单质制备W的气态氢化物的化学方程式是N2+3H2高温、高压催化剂 2NH3。
(2)若四种元素中只有一种金属元素,则根据元素在周期表中的相对位置可知,Y应该是金属,且是金属铝,W是B,X是C,Z是Si。
①铝是活泼的金属,通过电解熔融的氧化铝冶炼,反应的化学方程式是2Al2O3(熔融)
 4Al+3O2↑。
4Al+3O2↑。②工业上,将X的单质与Z的最高价氧化物加热到1900℃以上可制得一种新型陶瓷(ZX),同时得到一种可燃性气体,则根据原子守恒可知,该可燃性气体是CO,所以该反应的化学方程式是3C+SiO2
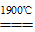 SiC+2CO↑。
SiC+2CO↑。③I. 由于乙酸是易挥发的,所以生成的CO2中含有乙酸,乙酸能干扰后续的实验,需要除去。除去CO2中的乙酸需要饱和碳酸氢钠溶液,即B试管中盛放的试剂是饱和NaHCO3溶液。
II. 要证明碳酸的酸性强于硅酸的,则C中应该盛放硅酸钠溶液,所以C试管中反应的化学方程式是Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3。
点评:该题是中等难度的试题,试题针对性强,贴近高考,难易适中。有利于培养学生规范的答题能力和实验设计能力,有利于提高学生的逻辑推理能力和应试能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力,考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 mol
mol mol
mol mol
mol