题目内容
【题目】KClO3和浓盐酸在一定温度下发生如(1)的反应:
(1)请配平方程式,并用双线桥表示得失电子情况: KClO3+HCl(浓)=KCl+ClO2↑+Cl2↑+H2O
(2)氧化剂是 , 还原产物是(写化学式).
(3)产生0.1molCl2时,转移电子的物质的量为mol.
【答案】
(1)2;4;2;2;1;2
(2)KClO3;ClO2
(3)0.2
【解析】解:(1)KClO3中氯元素化合价由+5价降低为ClO2中+4价,化合价降低1价;HCl中氯元素化合价由﹣1价升高为Cl2中0价,化合价升高2价,化合价升降最小公倍数为2,故ClO2系数为2,Cl2系数为1;所以KClO3系数为2,KCl系数为2,HCl系数为4,水的系数是2.电子转移的方向和数目为: 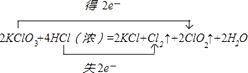 所以答案是:2;4;2;2;1;2;
所以答案是:2;4;2;2;1;2; 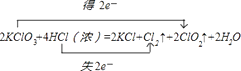 ;(2)KClO3中氯元素化合价降低,为氧化剂,对应生成ClO2为还原产物,所以答案是:KClO3;ClO2;(3)反应中只有Cl2是氧化产物,HCl中氯元素化合价由﹣1价升高为Cl2中0价,所以产生0.1molCl2 , 转移的电子的物质的量为0.1mol×2=0.2mol.
;(2)KClO3中氯元素化合价降低,为氧化剂,对应生成ClO2为还原产物,所以答案是:KClO3;ClO2;(3)反应中只有Cl2是氧化产物,HCl中氯元素化合价由﹣1价升高为Cl2中0价,所以产生0.1molCl2 , 转移的电子的物质的量为0.1mol×2=0.2mol.
所以答案是:0.2.

【题目】酶在酶促反应中能催化特定的底物(酶进行催化反应的反应物)反应,与酶的活性中心有关。酶的活性中心往往与底物分子在空间结构上具有特殊的匹配关系,当酶与底物结合时,启动化学反应的发生。请据图回答问题:

(1)上图所示过程能说明酶具有 的特点。
(2)酶能提高反应速率的机理是 ,使底物分子从常态转变为容易发生化学反应的活跃状态。
(3)下列符合图示反应类型的有 。
A.氨基酸a+氨基酸b→二肽+H2O
B.麦芽糖+H2O→葡萄糖
C.CO2+H2O→(CH2O)+O2
D.H2O2→H2O+O2
(4)请在下表中写出两个与酶有关的实验中的自变量:
序号 | 实验名称 | 自变量 | 因变量 |
① | 探索淀粉酶对淀粉和蔗糖水解的作用 | 加斐林试剂水浴加热,有无砖红色(沉淀)出现 | |
② | 研究温度对淀粉酶活性的影响 | 加碘后溶液颜色的变化 |
【题目】下图一是某课题组的实验结果(注:A酶和B酶分别是两种微生物分泌的纤维素酶)。请分析回答:

(1)分析图一的实验结果可知,本实验研究的课题是_____________。
(2)图一结果显示,在40℃至60℃范围内,热稳定性较好的酶是_____________。高温条件下,酶容易失活, 其原因是_______________。
(3)下表是图一所示实验结果统计表,由图一可知表中③处应是_____________,⑧处应是_____________。
温度(℃) | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
A酶活性(mmolS-1) | 3.1 | 3.8 | 5.8 | 6.3 | 5.4 | 2.9 | 0.9 |
B酶活性(mmolS-1) | 1.1 | 2.2 | 3.9 | ⑧ | 3.4 | 1.9 | 0 |
(4)图二表示30℃时B酶催化下的反应物浓度随时间变化的曲线,其他条件相同,在图二上画出A酶(浓 度与B酶相同)催化下的反应物浓度随时间变化的大致曲线。
(5)适宜条件下,取一支试管加入A酶和蛋白酶溶液并摇匀,一段时间后加入纤维素,几分钟后加入新制 斐林试剂并水浴加热,结果试管中没有产生砖红色沉淀,原因是_________________。
