题目内容
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.0.1mol·L-1Na2CO3溶液中Na+的数目为0.2NA
B.标准状况下,2.24LCCl4中的分子数目为0.1NA
C.常温常压下,17g氨气中所含氢原子数目为3NA
D.3.2g由O2和O3组成的混合物含有分子数目为0.1NA
【答案】C
【解析】
A.没有溶液体积,无法计算,A错误;
B.CCl4在标准状况下不是气体,不能用22.4L/mol计算,B错误;
C.17g氨气有1mol,每个氨气分子中有3个氢原子,1mol氨气分子有氢原子3mol,C正确;
D.若3.2g全是O2,则分子的物质的量为0.1mol,若3.2g全是O3,则分子的物质的量为![]() mol,最后的结果应该是在两者之间,D错误;
mol,最后的结果应该是在两者之间,D错误;
答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】通常人们把拆开 1 mol 某化学键所消耗的能量看作是该化学键的键能。键能的大小可衡量化学键的强弱,也可以估算化学反应的反应热。下表为某些化学键的键能
化学键 | N-N | O=O | N≡N | N-H |
键能(kJ/mol) | 154 | 500 | 942 | a |
已知火箭燃料肼(![]() )的有关化学反应的能量变化如图所示,则下列说法错误的是( )
)的有关化学反应的能量变化如图所示,则下列说法错误的是( )
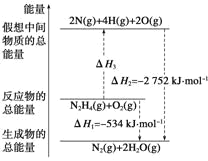
A.N2比O2稳定
B.N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-534 kJ/mol
C.表中的 a=194
D.图中的 ΔH3=+2218 kJ/mol