题目内容
20. 燃煤产生的烟气中的氮氧化物NOx(主要为NO、NO2)易形成污染,必须经脱除达标后才能排放.
燃煤产生的烟气中的氮氧化物NOx(主要为NO、NO2)易形成污染,必须经脱除达标后才能排放.(1)用化学方程式表示NO形成硝酸型酸雨的反应2NO+O2═2NO2、3NO2+H2O═2HNO3+NO.
(2)能作脱除剂的物质很多,下列说法正确的是ab.
a.用 H2O作脱除剂,不利于吸收含氮烟气中的NO
b.用 Na2SO3作脱除剂,O2会降低Na2SO3的利用率
c.用CO作脱除剂,会使烟气中NO2的浓度增加
(3)尿素[CO(NH2)2]在一定条件下能有效将NOx转化为N2.
Ⅰ.已知可通过下列方法合成尿素:
2NH3(g)+CO2(g)?H2NCOONH4(s)△H=-159.5kJ/mol
H2NCOONH4(s)?CO(NH2)2(s)+H2O(l)△H=+28.5kJ/mol
①尿素释放出NH3的热化学方程式是CO(NH2)2(s)+H2O(l)?2NH3(g)+CO2(g)△H=+131.0kJ/mol.
②写出有利于尿素释放NH3的条件并说明理由升高温度;升高温度有利于平衡向吸热反应方向进行,同时温度升高,氨气的溶解度降低,均有利于向释放氨气的方向进行.
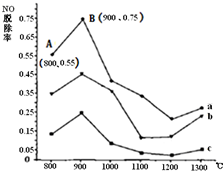
Ⅱ.CO(NH2)2与某种烟气(主要为N2、NO和O2)中的NO的物质的量比值分别为1:2、2:1、3:1时,NO脱除率随温度变化的曲线如图:
①曲线a 对应CO(NH2)2 与NO的物质的量比值是3:1.
②曲线a、b、c中,800℃~900℃区间内发生主要反应的化学方程式是4NH3+6NO═5N2+6H2O或2CO(NH2)2+6NO═2CO2+4H2O+5N2.
③900℃~1200℃区间内脱除率下降,NO浓度上升.发生的主要反应是4NH3+5O2═4NO+6H2O.
④曲线a中,NO的起始浓度为6×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为1.5×10-4mg/(m3•s).
分析 (1)一氧化氮不稳定,易和氧气反应生成二氧化氮,二氧化氮和水反应生成硝酸和一氧化氮;
(2)a.一氧化氮不易溶于,而二氧化氮易溶于水,反应生成NO;
b.亚硫酸钠不稳定,易被氧气氧化;
C.用CO作脱除剂,则氮氧化物得电子发生还原反应;
(3)Ⅰ. ①根据盖斯定律,将两个热化学方程式相加,然后进行颠倒即得目标方程式,其焓变进行相应改变;
②尿素释放NH3的反应是吸热反应,根据温度对化学平衡及氨气溶解度的影响进行分析;
Ⅱ.①CO(NH2)2 的含量越高,NO脱除率越高;
②、800℃~900℃区间内NO脱除率增大,NO参加反应,即尿素与NO反应生成N2;
③、900℃~1200℃区间内脱除率下降,NO浓度上升,反应中应该生成NO;
④、A点到BNO脱除率由0.55变为0.75,故NO的浓度变化量为(0.75-0.55)×6×10-4 mg/m3=1.2×10-4 mg/m3,再利用$\frac{浓度变化量}{时间}$计算NO的脱除速率.
解答 解:(1)一氧化氮不稳定,易和氧气反应生成二氧化氮,二氧化氮和水反应生成硝酸和一氧化氮,故NO形成硝酸型酸雨的反应为:2NO+O2═2NO2、3NO2+H2O═2HNO3+NO,故答案为:2NO+O2═2NO2、3NO2+H2O═2HNO3+NO;
(2)a.一氧化氮不易溶于,而二氧化氮易溶于水,反应生成NO,不利于吸收含氮烟气中的NO,故a正确;
b.亚硫酸钠不稳定,易被氧气氧化,O2会降低Na2SO3的利用率,故b正确;
C.用CO作脱除剂,被氧化,则氮氧化物得电子发生还原反应,不会生成NO2,烟气中NO2的浓度不增加,故c错误;
故答案为:ab;
(3)①已知:2NH3(g)+CO2(g)?H2NCOONH4(s)△H=-159.5kJ/mol
H2NCOONH4(s)?CO(NH2)2(s)+H2O(l)△H=+28.5kJ/mol
根据盖斯定律,两热化学方程式相加得2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(l)△H=-131kJ/mol,
故尿素释放出NH3的热化学方程式为:CO(NH2)2(s)+H2O(l)?2NH3(g)+CO2(g)△H=+131kJ/mol,
故答案为:CO(NH2)2(s)+H2O(l)?2NH3(g)+CO2(g)△H=+131kJ/mol;
②释放氨气的反应是吸热反应,升高温度,有利于平衡向吸热反应方向进行,同时温度升高,氨气的溶解度降低,均有利于向释放氨气的方向进行,
故答案为:升高温度;升高温度有利于平衡向吸热反应方向进行,同时温度升高,氨气的溶解度降低,均有利于向释放氨气的方向进行;
Ⅱ.①CO(NH2)2 的含量越高,NO的转化率越大,即NO脱除率越高,所以曲线a 对应CO(NH2)2 与NO的物质的量比值是3:1,
故答案为:3:1;
②800℃~900℃区间内NO脱除率增大,所以NO是作为反应物参加反应,高温时,尿素分解生成氨气、二氧化碳,氨气和一氧化氮发生氧化还原反应生成氮气,即尿素与NO反应生成N2,同时生成二氧化碳和水,所以反应方程式为:4NH3+6NO═5N2+6H2O 或 2CO(NH2)2+6 NO═2CO2+4H2O+5N2,
故答案为:4NH3+6NO═5N2+6H2O 或 2CO(NH2)2+6 NO═2CO2+4H2O+5N2;
③900℃~1200℃区间内脱除率下降,所以NO浓度上升,则该反应中应该有NO,尿素分解生成的氨气和烟气中的氧气反应生成一氧化氮和水,导致NO浓度增大,所以反应方程式为:4NH3+5O2═4NO+6H2O,
故答案为:4NH3+5O2═4NO+6H2O;
④A点到BNO脱除率由0.55变为0.75,故NO的浓度变化量为(0.75-0.55)×6×10-4 mg/m3=1.2×10-4 mg/m3
所以NO的脱除速率=$\frac{1.2×1{0}^{-4}mol/L}{0.8s}$=1.5×10-4mg/(m3.s),
故答案为:1.5×10-4.
点评 本题考查氮的化合物及其性质、盖斯定律在热化学方程式计算中的应用,题目难度中等,注意尿素加热时会分解生成氨气,且尿素是有机氮肥,正确分析图象是解本题的关键,注意图象中的曲线趋向和转折点,试题知识点较多、综合性较强,充分考查了学生的分析、理解能力及化学实验、化学计算能力.

 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案| A. | 漂粉精的主要成分:CaCl2 | |
| B. | 乙烯的结构简式:CH2=CH2 | |
| C. | Na+的结构示意图: | |
| D. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O |
| A. | 化学家可以制造出自然界中不存在的物质 | |
| B. | 化学的特征就是认识分子和制造分子,是一门具有创造性和实用性的科学 | |
| C. | 利用化学变化可以制造出新的分子,但不能制造出新的原子 | |
| D. | 化学研究会造成严重的环境污染,最终人类将会毁灭在化学物质中 |
| A. | Na+ Ba2+ Cl- SO42- | B. | K+ AlO2- NO3-OH- | ||
| C. | H+ NH4 + Al3+ SO42- | D. | H+ Cl- CH3COO- NO3- |
| A. | 萃取操作可在普通漏斗中完成 | |
| B. | 浓烧碱液沾到皮肤上应立即用稀盐酸冲洗 | |
| C. | 用酒精灯加热试管内液体时一定要先给试管预热再集中加热液体部位 | |
| D. | 用托盘天平称出25.20g氯化钠 |
| A. | 完全反应后所得溶液具有漂白性 | B. | 只发生了氧化还原反应 | ||
| C. | 会产生有刺激性气味的气体SO2 | D. | 溶液中存在HSO3- |
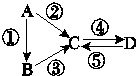 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图的反应关系: A、B、C、D、E、F为原子序数依次增大的短周期元素,G为第四周期元素,B、C相邻且同周期,A、D同主族.A、C能形成两种化合物甲和乙,原子个数比分别为2:1和1:1,甲为常见的溶剂.E是地壳中含量最多的金属元素.F元素为同周期电负性最大的元素.D和F可形成化合物丙,E和F可形成化合物丁.G为第四周期未成对电子数最多的元素.请回答下列问题:
A、B、C、D、E、F为原子序数依次增大的短周期元素,G为第四周期元素,B、C相邻且同周期,A、D同主族.A、C能形成两种化合物甲和乙,原子个数比分别为2:1和1:1,甲为常见的溶剂.E是地壳中含量最多的金属元素.F元素为同周期电负性最大的元素.D和F可形成化合物丙,E和F可形成化合物丁.G为第四周期未成对电子数最多的元素.请回答下列问题: