题目内容
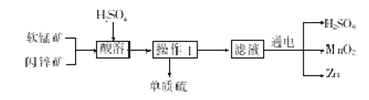
【题目】工业上用软锰矿(主要成分为MnO2)和闪锌矿(主要成分为ZnS)制取干电池中所需的MnO2和Zn的工艺流程如下,下列说法正确的是
A.酸溶时,ZnS作氧化剂
B.硫酸可以循环使用
C.可用盐酸代替硫酸进行酸溶
D.MnO2和ZnS均属于盐
【答案】B
【解析】
试题分析:A.软锰矿(主要成分为MnO2)和闪锌矿(主要成分为ZnS)在酸溶后生成了硫单质,说明二氧化锰做氧化剂,错误;B.根据图示可知用硫酸溶解软锰矿和闪锌矿,得到硫酸锰、硫酸锌,在后边电解溶液时又产生了硫酸,可以再用于溶解软锰矿和闪锌矿,因此硫酸可以循环使用,正确;C.盐酸代替硫酸进行酸溶,盐酸溶液中氯离子被氧化生成氯气,错误;D.MnO2是氧化物,不属于盐,错误。

【题目】(1)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于______________;
(2)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是______________(填“极性”或“非极性”)分子.
(3)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4______________H3PO4; HClO4______________HClO3;
(4)A和B的单质单位质量的燃烧热大,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
电离能(kJ/mol) | I1 | I2 | I3 | I4 |
A | 932 | 1821 | 15390 | 21771 |
B | 738 | 1451 | 7733 | 10540 |
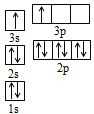
①某同学根据上述信息,推断B的核外电子排布如图所示,该同学所画的电子排布图违背了______________;
②根据价层电子对互斥理论,预测A和氯元素形成的简单分子空间构型为______________。