题目内容
10.下列说法正确的是( )| A. | 乙烯能使溴水和酸性高锰酸钾溶液褪色,其褪色原理相同 | |
| B. | 甲烷与氯气在光照条件下的反应属于置换反应 | |
| C. | 工业上可以通过乙烯与氯气发生加成反应制取氯乙烷 | |
| D. | 除去乙烷中的乙烯得到纯净的乙烷,可依次通过KMnO4(H+)溶液、NaOH溶液和H2SO4(浓) |
分析 A.乙烯含有碳碳双键,可发生加成、氧化反应;
B.甲烷和氯气发生取代反应;
C.工业用乙烯和氯化氢制备氯乙烷;
D.乙烯被氧化生成二氧化碳,二氧化碳与氢氧化钠反应,干燥后得到乙烷.
解答 解:A.乙烯含有碳碳双键,可与溴水发生加成反应,与酸性高锰酸钾发生氧化还原反应,故A错误;
B.甲烷和氯气反应生成氯代烃和HCl,为取代反应,因没有单质生成,不是置换反应,故B错误;
C.工业用乙烯和氯化氢制备氯乙烷,氯气与乙烯生成1,2-二氯乙烷,故C错误;
D.乙烯被氧化生成二氧化碳,二氧化碳与氢氧化钠反应,干燥后得到乙烷,故D正确.
故选D.
点评 本题综合考查元素化合物知识,为高频考点和常见题型,侧重于学生的分析能力和双基的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
18.已知某溶液中可能含有NH4+、SO32-、SO42-、NO3-及其它某些未知离子,某学生取适量试液放入试管中,然后进行如下实验并得出相应的结论,其中合理的是( )
| A. | 加入BaCl2溶液得到白色,过滤并洗涤沉淀,然后将沉淀加入到足量的稀硝酸中,沉淀无任何变化,说明该溶液中一定含有SO42- | |
| B. | 加入BaCl2溶液得到白色,过滤并洗涤沉淀,然后将沉淀加入到足量的稀盐酸中,沉淀溶解并产生刺激性气味的气体,说明该溶液中一定含有SO32- | |
| C. | 加入1mL0.2mol/L的NaOH,将湿润的紫色石蕊试纸靠近试管口,试纸无变化,说明溶液中一定无NH4+ | |
| D. | 加入锌片后无变化,再加入适量的稀硫酸,锌片溶解并有气泡产生,该溶液中一定含有NO3- |
5.物质的量浓度均为0.1mol•L-1的四种溶液:①NH4Cl溶液,②NH4HSO4溶液,③CH3COONH4溶液,④氨水,其c(NH4+)从大到小的顺序为( )
| A. | ②①③④ | B. | ①②③④ | C. | ④②①③ | D. | ①②④③ |
2.下列有机物名称中,错误的是( )
| A. | 1,2-二溴乙烷 | B. | 2,3-二甲基丁烷 | ||
| C. | 2-丁烯 | D. | 2-甲基-3-乙基丁烷 |
20.已知:CO(g)+$\frac{1}{2}$O2(g)=CO2(g);△H=-283kJ/mol
Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g);△H=-226kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g);△H=-226kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
| A. | CO的燃烧热为283kJ | |
| B. | 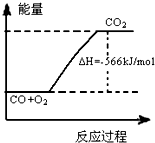 如图可表示由CO生成CO2的反应过程和能量关系 | |
| C. | Na2O2(s)+CO(g)=Na2CO3(s);△H=-509kJ/mol | |
| D. | Na2O2(s)与CO2(g)反应放出226kJ热量时,电子转移数为2NA |

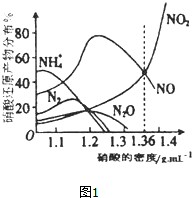 如图1是各种不同密度的硝酸与铁反应(相同温度)时主要还原产物的分布图.请认真读图分析,回答有关问题.
如图1是各种不同密度的硝酸与铁反应(相同温度)时主要还原产物的分布图.请认真读图分析,回答有关问题.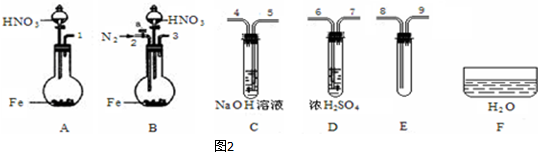
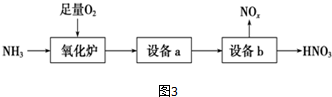
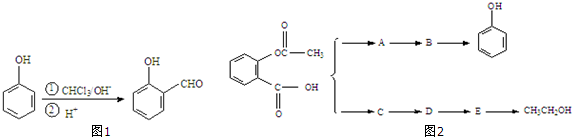
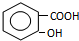 ,B
,B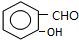 ,C
,C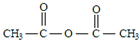 ,DCH3COOH,ECH3CHO.
,DCH3COOH,ECH3CHO.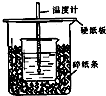 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: