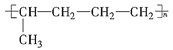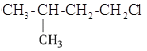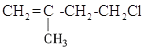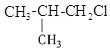题目内容
【题目】下列关于元素周期律的叙述正确的是( )
A.随着元素原子序数的递增,原子最外层电子数从1到8(第1周期元素及过渡元素除外)重复出现
B.随着元素原子序数的递增,元素最高正化合价从+1到+7、负化合价从-7到-1重复出现
C.随着元素原子序数的递增,原子(稀有气体元素原子除外)半径从小到大发生周期性变化
D.元素性质的周期性变化是元素原子核外电子排布周期性变化的必然结果
【答案】AD
【解析】
A.除了过渡元素以及第一周期原子最外层电子从1到2外,随着元素原子序数的递增,原子最外层电子总是从1到8重复出现,A正确;
B.随着元素原子序数的递增,主族元素(![]() 、
、![]() 除外)最高正化合价从
除外)最高正化合价从![]() 到
到![]() 、负化合价从
、负化合价从![]() 到
到![]() 重复出现,B错误;
重复出现,B错误;
C.除了稀有气体元素原子外,同周期半径从左向右在增大,同主族从上到下原子半径在增大,则同一周期(或主族)元素从左(上)到右(下),原子半径逐渐减小,呈现周期性变化,C错误;
D.元素的性质随着原子序数的递增而周期性变化的规律叫元素周期律,其实质是元素原子的核外电子排布周期性变化的必然结果,D正确;故答案为:AD。

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案【题目】氟代硼酸钾(KBe2BO3F2)是激光器的核心材料,我国化学家在此领域的研究走在了世界的最前列。回答下列问题:
(1)氟代硼酸钾中各元素原子的第一电离能大小顺序是F>O>____________。基态K+电子占据最高能级的电子云轮廓图为________形。
(2)NaBH4是有机合成中常用的还原剂,其中的阴离子空间构型是_______,中心原子的杂化形式为_______。NaBH4中存在_____(填标号)。
a. 离子键 b.氢键 c.σ键 d.π键
(3)BeCl2中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的BeCl2的结构式为________,其中Be的配位数为_______。
(4)第三周期元素氟化物的熔点如下表:
化合物 | NaF | MgF2 | AlF3 | SiF4 | PF5 | SF6 |
熔点/℃ | 993 | 1261 | 1291 | -90 | -83 | -50.5 |
解释表中氟化物熔点变化的原因:_____________________。
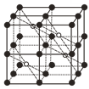
(5)CaF2的一种晶胞如图所示。Ca2+占据F-形成的空隙,其空隙率是________。若r(F-)=xpm,r(Ca2+)=ypm,设阿伏加德罗常数的值为NA,则CaF2的密度ρ=_________ g·cm-3(列出计算表达式)。