题目内容
【题目】在一定温度下,改变反应物中n(SO2)对反应2SO2(g)+O2(g)2SO3(g) △H<0的影响如图所示,下列说法正确的是
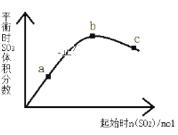
A.a、b、c三点中,平衡时的速率大小关系:v(b)>v(c)>v(a)
B.a、b、c三点中,a点时SO2的转化率最高
C.上述图象可以得出SO2的含量越高得到的混合气体中SO3的体积分数越高
D.a、b、c三点的平衡常数Kb>Kc>Ka
【答案】B
【解析】
根据题中反应2SO2(g)+O2(g)2SO3(g) △H<0可知,本题考查化学平衡图像,运用勒夏特列原理和化学平衡常数只与温度有关分析。
A.浓度越大,反应速率越快,则a、b、c三点反应速率大小为:vc>vb>va,故A错误;
B.曲线上的点为平衡状态,二氧化硫越少,氧气越多,则二氧化硫的转化率越大,a点时SO2的转化率最大,故B正确;
C.由图像知,随起始时![]() 的增大,平衡时
的增大,平衡时![]() 的体积分数先逐渐增大、后又逐渐减小,故C错误;
的体积分数先逐渐增大、后又逐渐减小,故C错误;
D.温度不变,则平衡常数不变,a、b、c三点平衡常数:Kb=Kc=Ka,故D错误;
答案选B。

练习册系列答案
相关题目