题目内容
20.已知:铅蓄电池总的化学方程式为:Pb+PbO2+2H2SO4=2H2O+2PbSO4;镍镉碱性充电电池在放电时,其正极反应为:2NiO(OH)+2H2O+2e-=2Ni(OH)2+2OH-负极反应为:Cd+2OH--2e-=Cd(OH)2
铅蓄电池使用(放电)一段时间后,其内阻明显增大,电压却几乎不变,此时只有充电才能继续使用.镍镉碱性充电电池使用(放电)到后期,当电压明显下降时,其内阻却几乎不变,此时充电后也能继续使用.回答下列问题:
(1)铅蓄电池在放电时的负极反应为Pb+SO42--2e-=PbSO4,其在充电时阳极反应为PbSO4+2H2O-2e-=PbO2+SO42-+4H+;
(2)镍镉碱性充电电池在充电时的总反应的化学方程式为Cd(OH)2+2Ni(OH)2=Cd+2NiO(OH)+2H2O;
(3)上述两种电池使用一段时间后,一个内阻明显增大,而另一个内阻却几乎不变的主要原因可能是铅蓄电池放电时离子浓度减小,而镍镉电池放电时离子浓度不变;
(4)如果铅蓄电池在放电时回路中有2mol电子转移时,消耗H2SO42mol.
分析 (1)依据铅蓄电池的总反应方程式中元素化合价变化判断,负极失电子发生氧化反应;正极得到电子发生还原反应,负极 Pb+SO42-=PbSO4+2e-;正极 PbO2+4H++SO42-+2e-=PbSO4+2H2O;
(2)依据放电时的电极反应,充电时是电解,原电池的正极接电源正极做阳极,原电池负极接电源负极,做电解池的阴极;综合写出电解反应;
(3)依据两种电池的电极反应过程中离子浓度变化分析判断;
(4)依据电极反应或电池反应中电子守恒计算得到.
解答 解:(1)铅蓄电池总的化学方程式为:Pb+PbO2+2H2SO4 $?_{充电}^{放电}$2H2O+2PbSO4;铅失电子生成硫酸铅,二氧化铅得到电子发生还原反应生成硫酸铅;负极电极反应为:Pb+SO42--2e-=PbSO4,正极电极反应为:PbSO4+2H2O-2e-=PbO2+SO42-+4H+;
故答案为:Pb+SO42--2e-=PbSO4;PbSO4+2H2O-2e-=PbO2+SO42-+4H+;
(2)镍镉碱性充电电池在放电时,
正极反应为:2NiO(OH)+2H2O+2e-=2Ni(OH)2+2OH-,
充电为阳极电极反应为:2Ni(OH)2+2OH--2e-=2NiO(OH)+2H2O;
负极反应为:Cd+2OH--2e-=Cd(OH)2,
充电为阴极电极反应为:Cd(OH)2+2e-=Cd+2OH-
电子守恒合并得到:Cd(OH)2+2Ni(OH)2=Cd+2NiO(OH)+2H2O;
故答案为:Cd(OH)2+2Ni(OH)2=Cd+2NiO(OH)+2H2O;
(3)两种电池使用一段时间后,一个内阻明显增大,而另一个内阻却几乎不变,阳极电极反应分析说明,铅蓄电池放电时离子浓度减小,而镍镉电池放电时离子浓度不变;
故答案:铅蓄电池放电时离子浓度减小,而镍镉电池放电时离子浓度不变;
(4)如果铅蓄电池在放电时回路中有2mol电子转移时,依据Pb+PbO2+2H2SO4 $?_{充电}^{放电}$2H2O+2PbSO4,2mol硫酸反应电子转移为2mol;
故答案为:2.
点评 本题考查了原电池的原理应用和电解原理应用,电极反应、电极判断、电池反应是解题关键,题目难度中等.

| A. | 稀硫酸滴加在铜片上:Cu+2H+═Cu2++H2↑ | |
| B. | 氢氧化镁溶解于盐酸:OH?+H+═H2O | |
| C. | 金属铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 铜和硝酸银溶液反应:Cu+2Ag+═2Ag+Cu2+ |
| A. | Cl2 | B. | HCl | C. | BaCO3 | D. | SO2 |
| A. | SO2 | B. | C2H4 | C. | 苯 | D. | NaOH |
| A. | CH4 | B. | C3H8 | C. | C10H20 | D. | C5H12 |
| A. | K[Ag(CN)2]、[Cu(NH3)4]SO4 | B. | [Ag(NH3)2]Cl、K[Ag(CN)2] | ||
| C. | [Ag(NH3)2]Cl、[Cu(NH3)4]SO4 | D. | [Ni(NH3)4]Cl2、[Ag(NH3)2]Cl |
| A. | 钇在周期表中的位置是第4周期ⅢB族 | |
| B. | 属于非金属元素 | |
| C. | 质子数与中子数之差为50 | |
| D. | 89Y和90Y是两种不同的核素 |

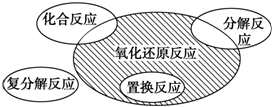 氧化还原反应和离子反应是中学化学中重要的反应类型.回答下列问题:
氧化还原反应和离子反应是中学化学中重要的反应类型.回答下列问题: =2Cr(OH)3↓+3O2↑+2H2O
=2Cr(OH)3↓+3O2↑+2H2O