题目内容
【题目】下列叙述正确的是( )
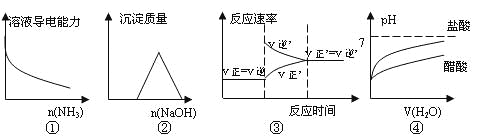
A.用水稀释0.1mol·L-1的氨水,则溶液中![]() 增大
增大
B.化学反应的反应热只与反应途径有关,而与反应体系的始态和终态无关
C.在等体积等pH的盐酸和醋酸两溶液中分别加入等质量的相同锌粒,若只有一种溶液中的锌粒有剩余,则该溶液一定是盐酸
D.两种氨水的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c2=10c1
【答案】C
【解析】
A. 用水稀释0.1mol·L-1的氨水,稀释过程中NH4+浓度逐渐减小,NH3H2O的电离平衡常数Kb不变,溶液中![]() 的值逐渐减小,A项错误;
的值逐渐减小,A项错误;
B. 反应热的大小取决于反应体系的始态和终态,与反应过程无关,B项错误;
C. pH相同的盐酸和醋酸,醋酸的浓度大于盐酸,等体积的两种酸,醋酸的物质的量大于盐酸,酸的物质的量越大,消耗的锌越多,若只有一种溶液中的锌粒有剩余,则该溶液一定是盐酸,C项正确;
D. 两种氨水的物质的量浓度分别为c1和c2,pH分别为a和a+1,氨水浓度越大其电离程度越小,因此c2>10c1,D项错误;
答案选C。

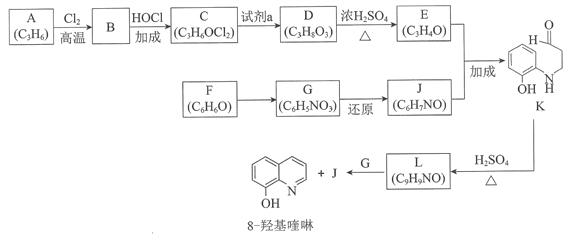
【题目】现有如下实验方案中,可以达到相应实验目的的是
A | B | C | D | |
方 案 |
|
|
|
|
目 的 | 验证不同催化剂对化学反应速率的影响 | 分离乙醇和水 | 将锌板换成铜板 对钢闸门保护效果更好 | 已知:Na2SiO3 + CO2 + H2O == Na2CO3 + H2SiO3↓ 验证非金属性:C > Si |
A. A B. B C. C D. D
【题目】在标准状况下进行甲、乙、丙三组实验。三组实验各取同浓度的盐酸30mL,加入同一种镁铝合金粉末,产生气体。有关数据列表如下(气体体积均为标准状况下测得):
实验序号 | 甲 | 乙 | 丙 |
合金质量/g | 0.255 | 0.385 | 0.459 |
生成气体/ml | 280 | 336 | 336 |
(1)该盐酸的物质的量浓度____________;
(2)合金中Mg、Al的物质的量之比为___________;
(3)在丙组实验后,向容器中加入1mol/L的NaOH溶液,恰好使合金中的铝元素全部转化为AlO2-,并使Mg2+刚好沉淀完全,则溶液中AlO2-的物质的量为__________mol;溶液中Na+的物质的量为_________mol;所加NaOH溶液的体积为_________mL。