��Ŀ����
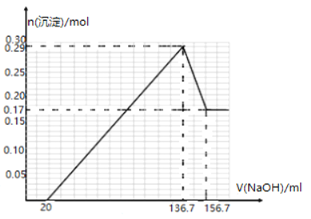
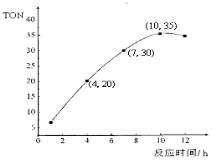
����Ŀ��ijϡ�����ϡ����Ļ��Һ25mL���������������ۣ�������������ʵ����������������ӵı仯��ͼ��ʾ(����Ļ�ԭ����ΪNO�����Է�Ӧ�е���Һ����仯)�������й�˵��������ǣ� ��

A.OA�β�����������NO��AB�η����ķ�ӦΪFe��2Fe3��=3Fe2����BC�β�����������H2
B.�ɴ��ƶϸ������£������ԣ�NO3-ǿ��Fe3��
C.OA����BC�β���������������Ϊ1��1
D.C�����ʵ����ʵ���Ũ��Ϊ10 mol��L-1
���𰸡�C
��������
��ͼ���֪��������������OA�η�����ӦΪ��Fe+NO3-+4H+=Fe3++NO��+2H2O��AB�η�����ӦΪ��Fe+2Fe3+=3Fe2+��BC�η�����ӦΪ��Fe+2H+=Fe2++H2������������14.0gFe����Һ������ΪFeSO4������FeԪ���غ���Լ���n(FeSO4)���ٸ���������غ����ÿһ����Һ��n(H2SO4)������������������ʵ���Ũ�ȡ�
A. ������������OA�η�����ӦΪ��Fe+NO3-+4H+=Fe3++NO��+2H2O��AB�η�����ӦΪ��Fe+2Fe3+=3Fe2+��BC�η�����ӦΪ��Fe+2H+=Fe2++H2������A��ȷ��
B. ��ͼ���֪��OA�η�����ӦΪ��Fe+NO3-+4H+=Fe3++NO��+2H2O��AB�η�����ӦΪ��Fe+2Fe3+=3Fe2+��Fe�Ⱥ�NO3-��Ӧ���ٺ�Fe3����Ӧ��˵�������ԣ�NO3-ǿ��Fe3������B��ȷ��
C. OA�η�����ӦΪ��Fe+NO3-+4H+=Fe3++NO��+2H2O������![]() =0.1molFe������0.1molNO��BC�η�����ӦΪ��Fe+2H+=Fe2++H2��������
=0.1molFe������0.1molNO��BC�η�����ӦΪ��Fe+2H+=Fe2++H2��������![]() =0.1molFe������0.1molH2��ѡ��û��˵����������ͬ��ͬѹ�£������ж�����ȣ���C����
=0.1molFe������0.1molH2��ѡ��û��˵����������ͬ��ͬѹ�£������ж�����ȣ���C����
D. ��������14.0gFe����Һ������ΪFeSO4��n(FeSO4)= n(Fe)=![]() =0.25mol�����ʵ���Ũ��Ϊ
=0.25mol�����ʵ���Ũ��Ϊ![]() =10mol/L����D��ȷ��
=10mol/L����D��ȷ��
��ѡC��

 ��У����ϵ�д�
��У����ϵ�д�