题目内容
【题目】在下列给定条件的溶液中,一定能大量共存的离子组是
A. 无色溶液:K+ 、Cl- 、 Mg2+、 SO42- 、Ag+
B. 能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3-
C. Na2CO3溶液:K+、Fe3+、SO42- 、NO3-
D. 常温下,Kw/c(H+)=0.1 mol/L的溶液:Na+、K+、SiO32-、NO3-
【答案】D
【解析】
A、Cl- 、SO42-与Ag+能反应生成沉淀;
B、能使pH试纸呈红色的溶液显酸性,I-有强还原性,NO3-在酸性溶液中有强氧化性,据此分析;
C、Fe3+与CO32-能发生双水解反应;
D、常温下,![]() = c(OH-) = 0.1 mol/L,为碱性溶液,据此分析作答。
= c(OH-) = 0.1 mol/L,为碱性溶液,据此分析作答。
A. Cl- 、SO42-与Ag+均能反应生成沉淀而不能大量共存,故A项错误;
B. 能使pH试纸呈红色的溶液显酸性,I和NO3在酸性溶液中能发生氧化还原反应而不能共存,故B项错误;
C. Fe3+水解显酸性,CO32水解显碱性,两者会发生双水解反应而不能共存,故C项错误;
D. 常温下,![]() = c(OH-) = 0.1 mol/L,可知该溶液为碱性溶液,该组离子与OH-相互间不反应,可以共存,故D项正确。
= c(OH-) = 0.1 mol/L,可知该溶液为碱性溶液,该组离子与OH-相互间不反应,可以共存,故D项正确。
答案选D。

 智慧小复习系列答案
智慧小复习系列答案【题目】B. [实验化学]
乙酰苯胺具有退热镇痛作用,是较早使用的解热镇痛药,有“退热冰”之称。其制备原理如下:

已知:
①苯胺易被氧化;
②乙酰苯胺、苯胺和醋酸的部分物理性质如下表:
物质 | 熔点 | 沸点 | 溶解度(20 ℃) |
乙酰苯胺 | 114.3℃ | 305℃ | 0.46 |
苯胺 | -6℃ | 184.4℃ | 3.4 |
醋酸 | 16.6℃ | 118℃ | 易溶 |
实验步骤如下:
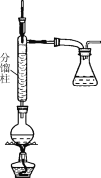
步骤1:在50 mL圆底烧瓶中,加入5 mL苯胺、7.5 mL冰醋酸及少许锌粉,依照如图装置组装仪器。
步骤2:控制温度计示数约105 ℃,小火加热回流1 h。
步骤3:趁热将反应混合物倒入盛有100 mL冷水的烧杯中,冷却后抽滤,洗涤,得到粗产品。
(1)步骤1中加入锌粉的作用是________。
(2)步骤2中控制温度计示数约105℃的原因是________。
(3)步骤3中趁热将混合物倒入盛有冷水的烧杯中,“趁热”的原因是__________________。抽滤装置所包含的仪器除减压系统外,还有________、________(填仪器名称)。
(4)步骤3得到的粗产品需进一步提纯,该提纯方法是________。


