��Ŀ����
����Ŀ�����º����£���2mol����A��2mol����Bͨ�����Ϊ2L���ܱ������У��������·�Ӧ��2A(g)+B(g)![]() xC(g)+2D(s)��2min��Ӧ�ﵽƽ��״̬����ʱʣ��1.2molB�������C��Ũ��Ϊ1.2mol/L��
xC(g)+2D(s)��2min��Ӧ�ﵽƽ��״̬����ʱʣ��1.2molB�������C��Ũ��Ϊ1.2mol/L��
��1���ӿ�ʼ��Ӧ���ﵽƽ��״̬������C��ƽ����Ӧ����Ϊ__��
��2��x=__��
��3�����и������Ϊ�÷�Ӧ�ﵽƽ��״̬�ı�־��__(����ĸ)��
A.�����ܶȲ��ٱ仯
B.ѹǿ���ٱ仯
C.A������������B����������֮��Ϊ2:1
D.����ƽ����Է����������ٱ仯
���𰸡�0.6mol��(L��min)-1 3 AD
��������
(1)C��Ũ�ȱ仯Ϊ1.2mol/L����������C��ƽ����Ӧ����Ϊ��![]() ��
��
(2)�з�Ӧ������ʽΪ��
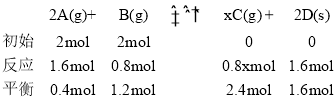
����x=3��
(3)A�������ܶȼ��㹫ʽ��![]() �����ܶȲ���ʱ��˵��
�����ܶȲ���ʱ��˵��![]() ���ٱ仯�����ڸ÷�Ӧ�IJ���D��Ϊ���壬���Դ�ʱ��Ӧһ��ƽ�⣬A����ȷ��
���ٱ仯�����ڸ÷�Ӧ�IJ���D��Ϊ���壬���Դ�ʱ��Ӧһ��ƽ�⣬A����ȷ��
B������x=3�����Է�Ӧǰ������������ʵ����㶨�����ݹ�ʽ��![]() �����º��ݵ������������ڵ�ѹǿ�㶨�����Ƿ�ƽ���أ�B�����
�����º��ݵ������������ڵ�ѹǿ�㶨�����Ƿ�ƽ���أ�B�����
C������A������B����ζ�ŷ�Ӧ������У���ˣ���֤��![]() ����Ӧ��һ��ƽ�⣬C�����
����Ӧ��һ��ƽ�⣬C�����
D������ƽ����Է��������ļ��㹫ʽΪ��![]() �����ڸ÷�Ӧ�������������㶨��������������������ŷ�Ӧ���з����仯�����Ե�
�����ڸ÷�Ӧ�������������㶨��������������������ŷ�Ӧ���з����仯�����Ե�![]() ����ʱ��˵�����������һ�����ٱ仯����ô�÷�Ӧһ������ƽ��״̬��D����ȷ��
����ʱ��˵�����������һ�����ٱ仯����ô�÷�Ӧһ������ƽ��״̬��D����ȷ��
��ѡAD��

����Ŀ����ʽ̼��ͭ������ľ�ķ�������ˮ��ɱ����ȣ��о���ѧϰС��������·����Ʊ���ʽ̼��ͭ���������ʵ��̽����
������ͭмΪԭ���Ʊ���ʽ̼��ͭ��װ�����£�
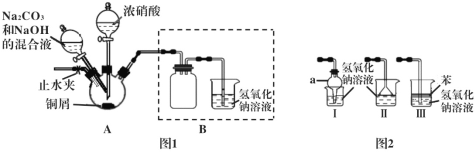
����1 ���Ӻ�װ�ã����װ�õ������ԣ�װҩƷ��
����2 ��������ƿ�м���������Ũ���ᣬʹͭм��ȫ��Ӧ��
����3 ������2��Ӧ�����Һ�м���һ��������Na2CO3��NaOH�Ļ��Һ�����ȡ�
����4 ��������ƿ�еĻ������ˡ�ϴ�ӡ���ɣ���ò��
��֪��������ʽ̼��ͭΪ����ɫ����ɫ�ᾧ��������ᣬ������ˮ����100���ˮ���ֽ⣻
����NO+NO2+2NaOH=2NaNO2+H2O��2NO2+2NaOH=NaNO3+NaNO2+H2O��
NO���ܵ�����NaOH��Һ��Ӧ��
��1������2��Ũ������ͭм��Ӧ�����ӷ���ʽΪ___________________��
��2������2��Ӧһ��ʱ������ֹˮ�У�ͨ��һ��ʱ��Ŀ�����Ŀ����_______��
��3������3��װ��A�ļ��ȷ�ʽ��ò���____________��
��4��װ����������a������Ϊ____��������װ�ò������ͼ1��Bװ�õ���_____����װ����ţ���
��5�������鲽��4��õIJ������Ƿ���NO3-��������Լ�������__________��
��̽����һ���¶��£���ͬ��ԭ����ȶԲ����Ӱ�죬ʵ���������£�
ʵ����� | V[Cu(NO3)2] /mL ��0.5 mo1��L-1�� | V(NaOH) / mL ��0.5 mo1��L-1�� | V(Na2CO3)/ mL ��0.25 mo1��L-1�� | �������� | ������ɫ |
1 | 2.0 | 2.0 | 1.6 | + | dz��ɫ |
2 | 2.0 | 2.0 | 2.0 | + + | dz��ɫ |
3 | 2.0 | 2.0 | 2.4 | + + + | ��ɫ |
4 | 2.0 | 2.0 | 2.8 | + + + | ��ɫ |
ע����+��Խ���ʾ������Խ��
��6�������������ݿɵã��Ʊ���ʽ̼��ͭ��ѵ�ԭ�����n[Cu(NO3)2]:n(NaOH) : n(Na2CO3) =___��
������ɵIJⶨ
��7����ʽ̼��ͭ�ijɷ��ж��֣���ѧʽ�ɱ�ʾΪmCu(OH)2��n CuCO3��Ϊ�ⶨ�������ü�ʽ̼��ͭ����ɣ�ѧϰС��ͬѧȷ��ȡ3.820 g��Ʒ���������������У���ˮ���l00 mL��Һ��ȡl0.00 mL��Һ����ƿ�У�������ˮϡ�ͣ�������ҺpH��3��4�����������KI��2 Cu2+ + 4 I- = 2 CuI�� + I2������0.l000 mol��L-1 Na2S2O3����Һ�ζ���2 S2O32- + I2 = 2I- + S4O62-�����ӽ��յ�ʱ���������ָʾ���������ζ����յ㣬��ɫ��ʧ������ƽ��ʵ����ƽ������Na2S2O3����Һ�����Ϊ35.00 mL���ü�ʽ̼��ͭ�Ļ�ѧʽΪ_____
����Ŀ����ͨ����н�������ʵ�飺
���� |
|
| |
���� | Fe�������������ɫ���ݣ�Һ���Ϸ���Ϊ����ɫ | Fe���������������ɫ ���ݺ�Ѹ��ֹͣ | Fe��Cu�Ӵ�������� ����������ɫ���� |
����˵���У�����ȷ���ǣ� ��
A.������������ɫ�����ɫ�Ļ�ѧ����ʽΪ��2NO+O2=2NO2
B.���е�����˵��Fe�����γ����ܵ������㣬��ֹFe��һ����Ӧ
C.�ԱȢ�������˵��ϡHNO3��������ǿ��ŨHNO3
D.��Ԣ���������Fe��Cu֮�����ӵ����ƣ����ж�Fe�Ƿ����������




