题目内容
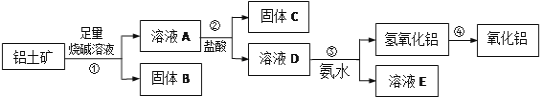
【题目】有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1mol E单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题:

(1)A元素的名称为_____,D离子的结构示意图为______
(2)C在周期表中的位置为_________
(3)B、C的气态氢化物的稳定性关系为______(填化学式)
(4)以上五种元素所形成的的最高价氧化物对应的水化物中,有一种物质既能与强酸反应又能与强碱反应,写出这种物质跟氢氧化钠溶液反应的化学方程式_________
【答案】氧 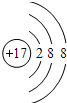 第三周期ⅥA族 PH3<H2S Al(OH)3+NaOH=Na[Al(OH)4]
第三周期ⅥA族 PH3<H2S Al(OH)3+NaOH=Na[Al(OH)4]
【解析】
A、B、C、D、E五种短周期元素,由位置图可以知道,A在第二周期,B、C、D处于第三周期,设C的质子数为x,则A的质子数为x-8,B的质子数为x-1,D的质子数为x+1,A、B、C、D四种元素原子核外共有56个电子,则x+(x-8)+(x-1)+(x+1)=56,计算得出x=16,故C为S,A为O,B为P,D为Cl;1mol E单质与足量酸作用,在标准状况下能产生33.6LH2,设E的化合价为y,根据电子转移守恒:1mol![]() y=
y=![]() 1,计算得出y=3,E的阳离子与A的阴离子核外电子层结构完全相同,则E为Al,然后利用元素及其单质、化合物的性质来解答。
1,计算得出y=3,E的阳离子与A的阴离子核外电子层结构完全相同,则E为Al,然后利用元素及其单质、化合物的性质来解答。
根据以上分析,A为O;B为P;C为S;D为Cl;E为Al,
(1)O元素的名称为氧,Cl-的结构示意图为 ,
,
因此,本题正确答案是:氧; ;
;
(2)S在周期表中的位置为第三周期ⅥA族,
因此,本题正确答案是:第三周期ⅥA族;
(3)元素的非金属性越强,其气态氢化物越稳定,P、S的非金属性P<S,则气态氢化物的稳定性关系为PH3<H2S,
因此,本题正确答案是:PH3<H2S;
(4)Al的最高价氧化物对应的水化物氢氧化铝是两性氢氧化物,既能与强酸反应又能与强碱反应,反应的化学方程式为Al(OH)3+NaOH=Na[Al(OH)4],
因此,本题正确答案是:Al(OH)3+NaOH=Na[Al(OH)4]。

 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案【题目】下表为元素周期表的一部分,参照元素①~在表中的位置,请回答下列问题。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
一 | ① | |||||||
二 | ② | ③ | ④ | ⑤ | ||||
三 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中元素,化学性质最稳定的是________,金属性最强的是__________,非金属性最强的是_______(写编号);最高价氧化物的水化物的酸性最强的是(写化学式)___________。
(2)④、⑩的气态氢化物中的稳定性强些的是_______。(填化学式)
(3)④、⑥、⑦、⑩元素形成的离子,离子半径的大小顺序是 ____________(填化学式)
(4)写出一种由①④组成且含有非极性键的物质的电子式_____________。
(5)实验室制取气体的离子方程式为_____________________________
(6)利用较强酸能制出较弱酸的原理,写出一个能证明②和⑧非金属性强弱的一个常见反应的化学方程式_______________。