题目内容
【题目】工业上可用O2将HCl转化为Cl2,反应为:O2(g)+4HCl(g)![]() 2Cl2(g)+2H2O(g)。请完成下列填空:
2Cl2(g)+2H2O(g)。请完成下列填空:
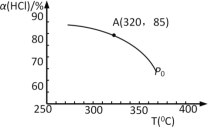
(1)该反应化学平衡常数K的表达式为_____________________;实验测得P0压强下,HCl平衡转化率α(HCl)随反应温度T的变化如图所示,则正反应是_________反应(填“吸热”或者“放热”)。
(2)写出一种能提高HCl转化率的方法___________________。
(3)上述实验中若压缩体积使压强由P0增大至P1,在图中画出P1压强下HCl平衡转化率α(HCl)随反应温度T变化的曲线______,并简要说明理由:_________________。
(4)根据图中信息所示,在P0、320℃条件下进行,达平衡状态A时,测得容器内n(Cl2)=7.2×10–3mol,则此时容器中n(HCl)=_____mol。
(5)氯元素能组成多种化合物,如常见的铵态氮肥,氯化铵溶液呈______性,其原因用离子方程式表示:___________________________。现有一瓶氯化铵、氯化钠和氨水的混合液,经测定溶液呈中性,此时三种离子的关系是:[Na+]+[NH4+]_____[Cl-](填“>”“<”或“=”)。
【答案】![]() 放热 增大氧气的浓度或加压或冷却后不断移去液态水
放热 增大氧气的浓度或加压或冷却后不断移去液态水 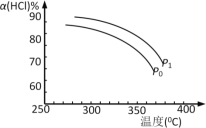 温度相同情况下,增大压强,平衡右移,HCl转化率增大 2.54×10–3 或2.5×10–3 酸 NH4++H2O
温度相同情况下,增大压强,平衡右移,HCl转化率增大 2.54×10–3 或2.5×10–3 酸 NH4++H2O![]() NH3H2O+H+ =
NH3H2O+H+ =
【解析】
(1);升高温度平衡向吸热的方向移动,据此判断。(2)可利用平衡移动的方法增大转化率。(3)正反应为气体体积减小的反应,增大压强,平衡向正反应方向移动,相同温度下HCl的平衡转化率比之前实验的大。(4)根据化学计量数中HCl与Cl2的关系,可算出状态A时HCl的变化量,再根据此时HCl的转化率可算出状态A时HCl的物质的量。(5)盐溶液的酸碱性要考虑盐的水解,溶液中离子浓度关系一般是电荷、物料、质子三个守恒。
(1)化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,根据化学平衡常数的概念可以写出其表达式为![]() ;由图可知,温度升高,HCl的转化率下降,说明平衡逆向移动,说明逆向是吸热,所以正反应是放热反应。
;由图可知,温度升高,HCl的转化率下降,说明平衡逆向移动,说明逆向是吸热,所以正反应是放热反应。
(2)增大氧气的浓度或加压或冷却后不断移去液态水等均能使平衡正向移动,提高HCl的转化率。
(3)正反应为气体体积减小的反应,增大压强,平衡向正反应方向移动,相同温度下HCl的平衡转化率比之前实验的大,所以P1压强下曲线在P0压强下曲线的上方(变化趋势与P0压强下曲线一致,都是温度越高,转化率越小)。
(4)根据反应方程式可知,HCl与Cl2的物质的量的变化量的关系为4:2,所以HCl的变化的物质的量为2n(Cl2)=1.44×10–2mol,由图可知此时HCl的转化率为85%,所以反应前HCl的起始物质的量为![]() ,所以此时HCl的物质的量为
,所以此时HCl的物质的量为![]() mol= 2.54×10–3mol。
mol= 2.54×10–3mol。
(5)因为铵离子水解:NH4++H2O![]() NH3H2O+H+,所以溶液显酸性;题目所给出的关系牵涉到的都是离子,所以可写出电荷守恒表达式c(NH4+)+c(Na+)+c(H+)= c(Cl-)+c(OH-),又因为溶液呈中性,所以c(NH4+)+c(Na+)=c(Cl-)。
NH3H2O+H+,所以溶液显酸性;题目所给出的关系牵涉到的都是离子,所以可写出电荷守恒表达式c(NH4+)+c(Na+)+c(H+)= c(Cl-)+c(OH-),又因为溶液呈中性,所以c(NH4+)+c(Na+)=c(Cl-)。