题目内容
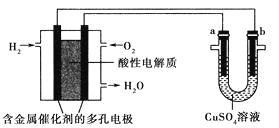
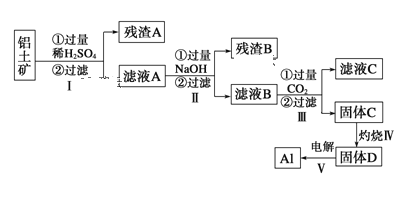
【题目】中科院某课题组将二氧化锰和生物质置于一个由滤纸制成的折纸通道内形成电池(如图所示),该电池可将可乐(pH=2.5)中的葡萄糖作为燃料获得能量。下列说法中正确的是( )
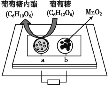
A. a极为正极
B. 随着反应不断进行,负极区的pH不断增大
C. b极电极反应式为MnO2+2H2O+2e-=Mn2++4OH-
D. 消耗0.01mol葡萄糖,电路中转移0.02mol电子
【答案】D
【解析】
A.失电子化合价升高的电极为负极,发生氧化反应;
B.负极区电极反应式为C6H12O6-2e-=C6H10O6+2H+,负极溶液中c(H+)增大;
C.b电极上二氧化锰得电子和氢离子反应生成水和Mn2+;
D.根据C6H12O6-2e-=C6H10O6+2H+计算转移电子物质的量。
A.根据图知,葡萄糖C6H12O6转化为葡萄糖内脂C6H10O6,C元素化合价由0价转化为+![]() ,则该电极上失电子发生氧化反应,所以a为负极,b为正极,A错误;
,则该电极上失电子发生氧化反应,所以a为负极,b为正极,A错误;
B.负极区电极反应式为C6H12O6-2e-=C6H10O6+2H+,负极溶液中c(H+)增大,则溶液的pH减小,B错误;
C.b电极上二氧化锰得电子和氢离子反应生成水和锰离子,电极反应式为MnO2+4H++2e-=Mn2++2H2O,C错误;
D.根据C6H12O6-2e-=C6H10O6+2H+可知,消耗1mol葡萄糖转移2mol电子,则消耗0.01mol葡萄糖转移0.02mol电子,D正确;
故合理选项是D。

【题目】t℃时,在体积不变的密闭容器中发生反应:X(g)+3Y(g)![]() 2Z(g),各组分在不同时刻的浓度如表,下列说法正确的是( )
2Z(g),各组分在不同时刻的浓度如表,下列说法正确的是( )
物质 | X | Y | Z |
初始浓度/mol/L | 0.1 | 0.2 | 0 |
2min末浓度/mol/L | 0.08 | a | b |
平衡浓度/mol/L | 0.05 | 0.05 | 0.1 |
A. 平衡时,X的转化率为20% B. t℃时,该反应的平衡常数为40
C. 增大平衡后的体系压强,v正增大,v逆减小,平衡向正反应方向移动 D. 前2min内,用Y的变化最表示的平均反应速率v(Y)=0.03mol/(L·min)