��Ŀ����
����Ŀ���ⱻ��Ϊ������Ԫ����,��ѧ�����ز����ɷ��ε�ȱ����,KI��KIO3���Ⱥ����ڼӵ����С�KI�������ڷ����Լ����й���ϡ���ҩ��,���Ʊ�ԭ������:
��ӦI : 3I2+ 6KOH== KIO3 +5KI+ 3H2O
��ӦII: 3H2S+KIO3=3S��+KI+ 3H2O
��ش��й����⡣
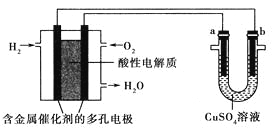
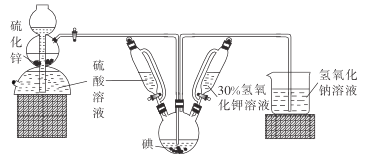
(1)���շ������з�����Ӧ�Ļ�ѧ����ʽΪ_______��װ����ʢװ30%����������Һ������������_________��
(2)�ر����շ���������,�ȵ���30%��KOH��Һ.���۲쵽������ƿ����Һ��ɫ���ػ�ɫ��Ϊ______(������) ,ֹͣ����KOH��Һ;Ȼ��______(�����),��������ƿ���ձ��в������ݵ����ʽӽ����ʱֹͣͨ����
(3)����������Һ,����������ƿ�е���Һ����ˮԡ����,��Ŀ����_____________��
(4)��������ƿ�е���Һ�����ձ���,����̼�ᱵ,�ڹ������й���,���˵õ��ij����г����й���̼�ᱵ��,���������ᱵ��___________(������)���ϲ���Һ��ϴ��Һ,�����������ᾧ������ó�Ʒ��
(5)ʵ����ģ�ҵ�Ʊ�KIO3��������:
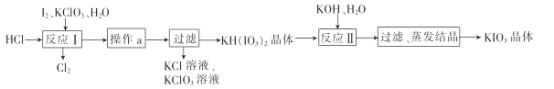
�������ʵ��ܽ�ȼ��±�:
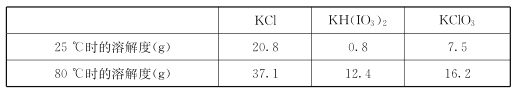
�����ϱ����ݷ�����֪��������a��Ϊ__________________��
���ö��Ե缫���KI��ҺҲ���Ʊ�KIO3,���ⷨ��ȣ����������Ʊ�KIO3��ȱ����____________��
(6)ijͬѧ�ⶨ.��������������KIO3��Ʒ�Ĵ��ȡ�
ȡ1.00 g��Ʒ��������ˮ�в��������ữ���ټ��������KI�������ĵ�����Һ����εμ�2.0 mol��L-1 Na2S2O3 ��Һ,ǡ����ȫ��Ӧʱ������12. 60 mL Na2S2O3��Һ������Ʒ��KIO3����������Ϊ_______(��֪��Ӧ:I2+2Na2S2O3=2NaI+Na2S4O6)��
���𰸡�ZnS+H2SO4===H2S��+ZnSO4 ��ѹ��Һ©�� ��ɫ �����շ�����������ͨ������ ʹ��Һ�ữ�����ȣ���������Һ��ʣ��������ݳ����Ӷ���ȥ���� �� ����Ũ������ȴ�ᾧ(���ؽᾧ) KClO3��I2��Ӧʱ������ж�����������Ⱦ������ 89.88%
��������
ʵ�����Ϊ���ȹر����շ�������������������ƿ�е���30%��KOH��Һ��������ӦI : 3I2+ 6KOH== KIO3 +5KI+ 3H2O�����ⵥ����ȫ��Ӧ��Ȼ������շ��������������շ��������������п��Ӧ�����������壬������ͨ��������ƿ�з�����ӦII: 3H2S+KIO3=3S��+KI+ 3H2O��������ػ�ԭ��KI������������Һ��������δ��Ӧ�����⣻
(5)ʵ����ģ�ҵ�Ʊ�KIO3����I2��HCl��KClO3ˮ�л�Ϸ���������ԭ��Ӧ������KH(IO3)2��֮���������Ũ������ȴ�ᾧ�����˵õ�KH(IO3)2���壬����KOH��Һ��Ϸ�����Ӧ�����������ᾧ�õ�����ؾ��塣
(1)���շ������з����ķ�Ӧ����п��ϡ���ᷴӦ�����������������п����Ӧ�Ļ�ѧ����ʽ��ZnS+H2SO4===H2S��+ZnSO4�����������ṹ��֪������Ϊ��ѹ��Һ©����
(2)�ⵥ��ˮ��Һ���ػ�ɫ�������������غ�ⵥ�ʷ�Ӧ���ɵ���غ͵⻯�أ���ȫ��Ӧ����Һ��Ϊ��ɫ��Ȼ������շ�����������ͨ�����巢����ӦII��
(3)��Ӧ��ɺ���Һ���������⣬�������Ტˮԡ���ȿɽ���������ܽ�ȣ�ʹ���ݳ����Ӷ���ȥ���⣻
(4)���ݷ�ӦII��֪��Ӧ���������������ɣ����ʲ�����ˮ��
(5)�ٸ��ݱ������ݿ�֪�¶Ƚϵ�ʱKH(IO3)2���ܽ�Ⱥ�С�����Դӻ��Һ�з���KH(IO3)2������Ҫ����Ũ������ȴ�ᾧ�����ˣ����Բ���aΪ����Ũ������ȴ�ᾧ��
�ڸ������̿�֪�ù����������������������ж�����Ⱦ������ͬʱ�ù����������˸����ҩƷ��
(6)�õζ�ԭ���ǣ��ȼ��������KI���ữ��KIO3������Ӧ��IO3 +5I+ 6H+===3I2+3H2O��Ȼ������Na2S2O3�ⶨ���ɵĵⵥ�ʵ����Ӷ�ȷ��KIO3���������ݷ�Ӧ����ʽ��֪IO3 ~3I2�����ݵζ����̷�ӦI2+2Na2S2O3===2NaI+Na2S4O6��֪I2~2Na2S2O3������IO3 ~6Na2S2O3������n(KIO3)=0.01260L��2.0mol/L��![]() =0.0042mol��������Ʒ��KIO3����������Ϊ
=0.0042mol��������Ʒ��KIO3����������Ϊ![]() =89.88%��
=89.88%��

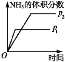
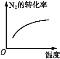
����Ŀ�����ڿ��淴ӦN2��g��+3H2��g��![]() 2NH3��g�� ��H<0,�����о�Ŀ�ĺ�ʾ��ͼ������ǣ�����
2NH3��g�� ��H<0,�����о�Ŀ�ĺ�ʾ��ͼ������ǣ�����
A | B | C | D | |
�о�Ŀ�� | ѹǿ�Է�Ӧ��Ӱ�죨p2>p1�� | �¶ȶԷ�Ӧ��Ӱ�� | ƽ����ϵ������N2��Ũ�ȶԷ�Ӧ��Ӱ�� | �����Է�Ӧ��Ӱ�� |
ʾ��ͼ |
|
|
|
|
A. AB. BC. CD. D