题目内容
14.已知四种元素A、B、C、D,其原子序数依次增大,最外层电子数依次为4、1、2、7,其中A元素原子次外层电子数为2,B、C 两元素的原子次外层电子数为8,B元素原子最外层电子数比第1层电子数少1,也比C元素原子第M层电子数少1,D元素的单质为液态非金属单质.若此四种元素均位于元素周期表前四个周期,请按要求填写下列各题:(1)A原子的原子结构示意图为
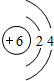 ,D元素在元素周期表中的位置为第四周期第ⅦA族.
,D元素在元素周期表中的位置为第四周期第ⅦA族.(2)B元素的最高价氧化物对应的水化物用电子式表示为
 ,C、D两元素形成的化合物化学键类型为离子键.
,C、D两元素形成的化合物化学键类型为离子键.(3)请写出D元素的单质与SO2同时通入水中反应的化学方程式:Br2+SO2+2H2O=2HBr+H2SO4.
分析 前四周期中A、B、C、D四种元素的原子序数依次增大,最外层电子数依次为4、1、2、7,其中A元素原子次外层电子数为2,则A为碳元素;B、C 两元素的原子次外层电子数为8,B元素原子最外层电子数比第1层电子数少1,也比C元素原子第M层电子数少1,则C元素原子M层电子数为2,则B为Na、C为Mg;D最外层电子数为7,为卤族元素,D元素的单质为液态非金属单质,则D为Br.
解答 解:前四周期中A、B、C、D四种元素的原子序数依次增大,最外层电子数依次为4、1、2、7,其中A元素原子次外层电子数为2,则A为碳元素;B、C 两元素的原子次外层电子数为8,B元素原子最外层电子数比第1层电子数少1,也比C元素原子第M层电子数少1,则C元素原子M层电子数为2,则B为Na、C为Mg;D最外层电子数为7,为卤族元素,D元素的单质为液态非金属单质,则D为Br.
(1)A为C元素,原子结构示意图为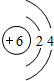 ,D为Br元素,在元素周期表中的位置为第四周期第ⅦA族,故答案为:
,D为Br元素,在元素周期表中的位置为第四周期第ⅦA族,故答案为: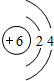 ;第四周期第ⅦA族;
;第四周期第ⅦA族;
(2)B元素的最高价氧化物对应的水化物为NaOH,电子式为: ,C、D两元素形成的化合物为MgBr2,含有离子键,故答案为:
,C、D两元素形成的化合物为MgBr2,含有离子键,故答案为: ;离子键;
;离子键;
(3)D元素的单质与SO2同时通入水中反应的化学方程式:Br2+SO2+2H2O=2HBr+H2SO4,故答案为:Br2+SO2+2H2O=2HBr+H2SO4.
点评 本题考查结构与位置关系,推断元素是解题关键,侧重对化学用语的考查,比较基础.

练习册系列答案
相关题目
3.常温下,在下列溶液中各组离子一定能够大量共存的是( )
| A. | 加入KSCN试液显红色的溶液中:K+、Na+、OH-、Cl- | |
| B. | 加入石蕊试液显蓝色的溶液中:K+、NH4+、NO3-、Cl- | |
| C. | 由水电离的c(H+)═1×10-14mol•L-1的溶液中:Na+、K+、Cl-、HCO3- | |
| D. | 向水中通入Cl2达到饱和的溶液中:Al3+、Cu2+、NO3-、SO42- |
4.海水开发利用的部分过程如图所示.下列说法错误的是( )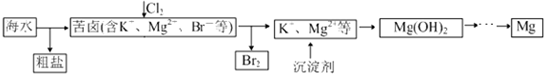

| A. | 粗盐可采用除杂和重结晶等过程提纯 | |
| B. | 向苦卤中通入Cl2 是为了提取溴 | |
| C. | 实际生产中常选用Ca(OH)2作为沉淀剂 | |
| D. | 工业生产中电解熔融氧化镁的方法制取镁 |
 如图所示,A、B、C、D、E 分别是铁、硝酸铜溶液、二氧化碳、稀硫酸溶液、氢氧化钠溶液中的一种,A是硝酸铜溶液(“-”相连两物质能发生反应).请回答:
如图所示,A、B、C、D、E 分别是铁、硝酸铜溶液、二氧化碳、稀硫酸溶液、氢氧化钠溶液中的一种,A是硝酸铜溶液(“-”相连两物质能发生反应).请回答: