题目内容
【题目】在国庆70周年庆典上,空中飞过的歼击机编队让我们热血沸腾,其中有中国自主研制的最先进的歼20隐形超音速飞机。当超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层,,或许通过测定局部的臭氧浓度变化可使飞机不再“隐形”。因此科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g) △H<0。请回答下列问题:
2CO2(g)+N2(g) △H<0。请回答下列问题:
(1)该反应的平衡常数表达式为___________________________。
(2)假设在闭容器发生上述反应,达到平衡后采取下列选项的措施既能加快反应速率又能提高NO转化率的是_____________。
A.选用更有效的催化剂同时增加CO的量 B.升高反应体系的温度
C.及时加入碱石灰 D.缩小容器的体积
(3)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学将等物质的量的NO和CO充入容积为2L的恒容密闭容器中,设计了三组实验,部分实验数据已经填在下面实验设计表中。
实验编号 | T/℃ | NO初始浓度/mol·L-1 | NO平衡浓度/mol·L-1 | 催化剂的比表面积/m2·g-1 |
Ⅰ | 280 | 0.3 | 0.1 | 82 |
Ⅱ | T1 | c1 | c2 | 124 |
Ⅲ | 350 | c3 | c4 | 124 |
①在上述表格的实验条件数据中,T1=____________,c3=_____________。
②平衡时若保持温度T1℃不变,再向容器中充入CO和CO2各0.2mol,则平衡将_________移动(填“向左”“向右”或“不”)
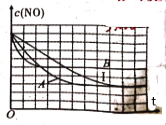
③在给出的坐标图中,画出了上表中的I、Ⅱ、Ⅲ实验条件下建立平衡过程中,混合气体里NO浓度随时间变化的趋势曲线图,请说出B曲线对应的实验编号__________(填Ⅱ、Ⅲ)。
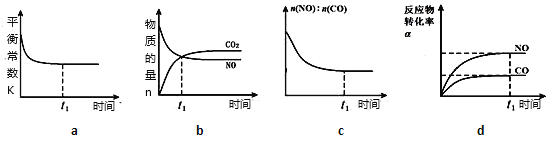
(4)在恒温恒容的密闭容器中通入n(NO):n(CO)=1:3的混合气体,发生上述反应,下列图像正确且能说明反应在进行到t1时刻一定达到平衡状态的是__________(选填字母)。
【答案】K=![]() A、D 280 0.3 向右 Ⅲ c、d
A、D 280 0.3 向右 Ⅲ c、d
【解析】
(1)根据平衡常数的公式结合题给的反应写出平衡常数表达式;
(2)措能加快反应速率的外界条件:增大浓度、升高温度、增大气体的压强、使用催化剂等;提高NO转化率的方法:增大压强,降低温度、增大一氧化碳浓度等;据以上分析解答。
(3)①根据控制变量法,在进行比较时,其他量不变,让一个量发生变化进行分析;
②由三段式计算出平衡常数K;根据浓度商与K的关系确定反应进行的方向。
③催化剂不影响平衡的移动,改变反应的速率;
(4)根据反应达到平衡状态时,正逆反应速率相等,各组分的浓度保持不变及由此衍生出的其它物理量进行分析。
(1)该反应的平衡常数表达式为K=![]() 。
。
(2)A.选用更有效的催化剂能加快反应速率,增大反应物的浓度,平衡正向移动,另一反应物的转化率提高,A项正确;
B.反应是个放热反应,升高体系的温度,平衡逆向移动,NO的转化率降低,B项错误;
C.碱石灰吸收二氧化碳,使产物二氧化碳浓度减小,并不能加快反应速率,C项错误;
D.缩小容器的体积,增大了压强,使反应速率加快,由于该反应正向是一个气体分子总数减小的反应,加压平衡正向移动,使一氧化NO转化率提高,D项正确;
答案选AD。
(3)①根据控制变量法,第Ⅰ组和第Ⅱ组比表面积不同,那温度就是相同的,所以T1是280℃,各组投放物料是一样的,故c3仍是0.3 mol·L-1。
②由三段式计算出平衡常数k:
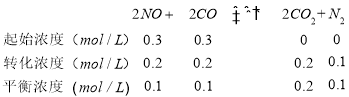
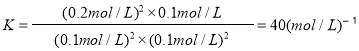 ,再向容器中充入CO和CO2各0.2mol,瞬间各物质的浓度:c(NO)=0.1 mol·L-1、C(CO)=0.2 mol·L-1、c(CO2)=0.3 mol·L-1、c(N2) =0.1mol·L-1。浓度商
,再向容器中充入CO和CO2各0.2mol,瞬间各物质的浓度:c(NO)=0.1 mol·L-1、C(CO)=0.2 mol·L-1、c(CO2)=0.3 mol·L-1、c(N2) =0.1mol·L-1。浓度商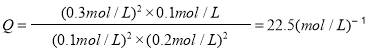
Q<K,故平衡正向移动。
③催化剂表面积的改变并不能影响到达平衡时平衡浓度,能够影响平衡移动的,在该题中是温度,B曲线到达平衡时的浓度和另外两条不一样,所以B曲线对应的是350℃即Ⅲ组的实验。
(4)a.平衡常数只受温度影响而改变,只要温度没变,无论是否达到平衡,平衡常数都不会改变,故t1时刻不能判断是否达平衡,a项错误;
b.t1时刻CO2和NO物质的量相等,但t1时刻之后CO2、NO物质的量还在改变,故t1时刻没有达到平衡状态,b项错误;
c.起始通入n(NO):n(CO)=1:3,二者反应按1:1进行转化,随反应进行比例关系发生变化,t1时刻起n(NO):n(CO)不变了,则说明已达平衡,故c项正确;
d.转化率不变了,说明已达到平衡,d项正确;
答案选c、d。