题目内容
【题目】
铜矿( CuFeS2)是炼铜的最主要矿物。火法冶炼黄钢矿的过程中,其中一步反应是:2Cu2O+Cu2S![]() 6Cu+SO2。回答下列问题。
6Cu+SO2。回答下列问题。
(1)Cu+价电子的电子排布图为___________,Cu2O与Cu2S比较,熔点较高的是___________,原因为______________________。
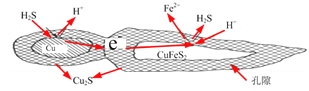
(2)SO2与SO3的键角相比,键角更小的是___________。某种硫的氧化物冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构片段如图1所示。此固态物质中S原子的杂化轨道类型是___________;该物质的化学式为___________。

(3)离子化合物CaC2的晶体结构如图2所示。写出该物质的电子式___________。从钙离子看该晶体属于___________堆积,一个晶胞含有的π键平均有___________个。

(4)根据图3可知,与每个C60分子距离最近且相等的C60分子有___________个,其距离为___________cm(列出计算式即可)。

【答案】![]() Cu2O 两物质均为离子化合物,且离子所带电荷数相同,O2-半径小于S2-,所以Cu2O的晶格能大,熔点更高 SO2 sp3 SO3或(SO3)n
Cu2O 两物质均为离子化合物,且离子所带电荷数相同,O2-半径小于S2-,所以Cu2O的晶格能大,熔点更高 SO2 sp3 SO3或(SO3)n ![]() 面心立方 8 12
面心立方 8 12 ![]()
【解析】
(1)Cu位于第四周期IB族,Cu+的价电子为第三层的d能级,根据泡利原理和洪特规则,书写价电子轨道式;Cu2O和Cu2S都属于离子晶体,晶格能越大,晶体熔沸点越高,据此分析作答;
(2)孤电子对之间的斥力>孤电子对-成键电子对之间的斥力>成键电子对之间斥力,据此分析键角大小;利用均摊法求出图1中的化学式组成,再请根据杂化轨道类型判断其杂化方式;
(3)碳化钙中存在离子键与非极性共价键,据此写出其电子式;结合金属原子常见堆积模型作答;再根据均摊法计算所含π键数目。
(1)Cu位于第四周期IB族,Cu+的价电子为第三层的d能级,根据泡利原理和洪特规则,Cu+价电子轨道式为![]() ;Cu2O和Cu2S都属于离子晶体,晶格能越大,晶体熔沸点越高,晶格能与半径、所带电荷数有关,半径越小、所带电荷数越多,晶格能越大,Cu2O和Cu2S所带电荷数相同,S2-的半径大于O2-的半径,因此Cu2S的沸点低于Cu2O;
;Cu2O和Cu2S都属于离子晶体,晶格能越大,晶体熔沸点越高,晶格能与半径、所带电荷数有关,半径越小、所带电荷数越多,晶格能越大,Cu2O和Cu2S所带电荷数相同,S2-的半径大于O2-的半径,因此Cu2S的沸点低于Cu2O;
故答案为![]() ;Cu2O;两物质均为离子化合物,且离子所带电荷数相同,O2-半径小于S2-,所以Cu2O的晶格能大,熔点更高;
;Cu2O;两物质均为离子化合物,且离子所带电荷数相同,O2-半径小于S2-,所以Cu2O的晶格能大,熔点更高;
(2)SO2含有的孤电子对为(6-2×2)/2=1,SO3中含有孤电子对为(6-2×3)/2=0,孤电子对之间的斥力>孤电子对-成键电子对之间的斥力>成键电子对之间斥力,因此SO3键角大于SO2键角;根据图1可知,该固体结构的基本单元中含S原子数目为1个,O原子数目为![]() =3个,所以其化学式为SO3或(SO3)n,又因为中心S有4个σ键,无孤电子对,价层电子对数为4,杂化轨道数等于价层电子对数,即杂化类型为sp3;
=3个,所以其化学式为SO3或(SO3)n,又因为中心S有4个σ键,无孤电子对,价层电子对数为4,杂化轨道数等于价层电子对数,即杂化类型为sp3;
故答案为SO2;sp3;SO3或(SO3)n;
(3)根据图2,CaC2的电子式为:![]() ;根据晶胞的结构,Ca2+位于顶点和面心,因此属于面心立方堆积;C22-位于棱上和体心,属于晶胞的C22-的个数为12×1/4+1=4,根据CaC2的电子式,两个碳原子之间有3对电子对,即1个C22-有2个π键,即1个晶胞中有2×4=8个π键;
;根据晶胞的结构,Ca2+位于顶点和面心,因此属于面心立方堆积;C22-位于棱上和体心,属于晶胞的C22-的个数为12×1/4+1=4,根据CaC2的电子式,两个碳原子之间有3对电子对,即1个C22-有2个π键,即1个晶胞中有2×4=8个π键;
故答案:![]() ;面心立方; 8。
;面心立方; 8。
(4)根据图3,与每个C60分子距离最近且相等的C60分子有12个,其距离等于边长的![]() ,所以其距离 =
,所以其距离 = ![]() ,
,
故答案为12;![]() 。
。

【题目】在国庆70周年庆典上,空中飞过的歼击机编队让我们热血沸腾,其中有中国自主研制的最先进的歼20隐形超音速飞机。当超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层,,或许通过测定局部的臭氧浓度变化可使飞机不再“隐形”。因此科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g) △H<0。请回答下列问题:
2CO2(g)+N2(g) △H<0。请回答下列问题:
(1)该反应的平衡常数表达式为___________________________。
(2)假设在闭容器发生上述反应,达到平衡后采取下列选项的措施既能加快反应速率又能提高NO转化率的是_____________。
A.选用更有效的催化剂同时增加CO的量 B.升高反应体系的温度
C.及时加入碱石灰 D.缩小容器的体积
(3)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学将等物质的量的NO和CO充入容积为2L的恒容密闭容器中,设计了三组实验,部分实验数据已经填在下面实验设计表中。
实验编号 | T/℃ | NO初始浓度/mol·L-1 | NO平衡浓度/mol·L-1 | 催化剂的比表面积/m2·g-1 |
Ⅰ | 280 | 0.3 | 0.1 | 82 |
Ⅱ | T1 | c1 | c2 | 124 |
Ⅲ | 350 | c3 | c4 | 124 |
①在上述表格的实验条件数据中,T1=____________,c3=_____________。
②平衡时若保持温度T1℃不变,再向容器中充入CO和CO2各0.2mol,则平衡将_________移动(填“向左”“向右”或“不”)
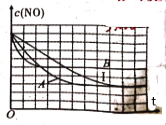
③在给出的坐标图中,画出了上表中的I、Ⅱ、Ⅲ实验条件下建立平衡过程中,混合气体里NO浓度随时间变化的趋势曲线图,请说出B曲线对应的实验编号__________(填Ⅱ、Ⅲ)。
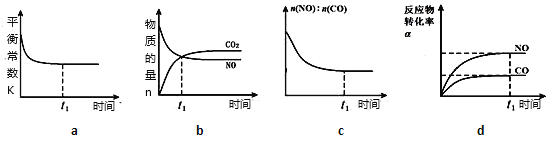
(4)在恒温恒容的密闭容器中通入n(NO):n(CO)=1:3的混合气体,发生上述反应,下列图像正确且能说明反应在进行到t1时刻一定达到平衡状态的是__________(选填字母)。