题目内容
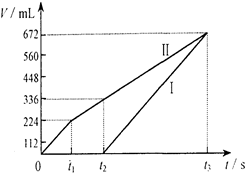
某金属元素R的硝酸盐R(NO3)n溶液用Pt电极电解,阳极产生气体V L(标准状况)时,阴极质量增加m g,若R的原子量为M,下列叙述中不正确的是 ( )
A.电路中通过电子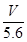 mol mol | B.n= |
C.溶液中H+增加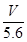 mol mol | D.n=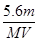 |
D
试题分析:根据电解时,得失电子数相等推断出金属与氧气的关系,从而确定金属的相对原子质量。
R的相对原子质量是M,则根据电解的方程式可知:
4R(NO3)n+2nH2O
 4R+nO2↑+4nHNO3
4R+nO2↑+4nHNO34Mg 22.4nL
mg VL
解得n=
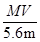 ,B正确,D不正确;
,B正确,D不正确;电路中通过电子的物质的量=
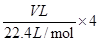 =
=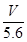 mol,A正确;
mol,A正确;溶液中生成硝酸的物质的量是
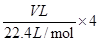 =
=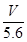 mol,C正确,答案选D。
mol,C正确,答案选D。点评:本题以电解原理为载体考查了氧化还原反应的有关计算,能正确写出该电池的电解反应式并找出金属与氧气的关系式是解本题的关键,要注意根据得失电子相等配平方程式,才能正确解答问题。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
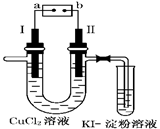

 沉淀完全,而在pH≥3.2时
沉淀完全,而在pH≥3.2时
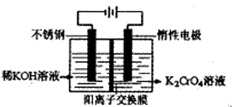
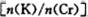 为d,则此时的铬酸钾的转化率为 。
为d,则此时的铬酸钾的转化率为 。 6Cu+SO2↑,反应的氧化剂是 。
6Cu+SO2↑,反应的氧化剂是 。