题目内容
4.羰基硫(COS)存在于许多种植物中,杀虫效果显著.它与CO2、CS2互为等电子体,已知C=O键的键能为745kJ•mol-1,有关硫化羰的说法正确的是( )| A. | 分子中有2个σ键和1个π键 | |
| B. | 可推测C=S键的键能大于745kJ•mol-1 | |
| C. | COS中碳原子是采用sp2杂化方式成键的 | |
| D. | 分解温度:CS2、COS、CO2依次由低到高 |
分析 A.羰基硫结构为S=C=O;
B.硫的电负性比氧弱;
C.根据中心原子上σ键的数目判断杂化类型;
D.电负性越大,成键的键能越大越稳定.
解答 解:A.羰基硫结构为S=C=O,分子中有2个σ键和2个π键,故A错误;
B.硫的电负性比氧弱,C=S键的键能小于745kJ•mol-1,故B错误;
C.COS中碳原子上含有2个σ键电子对,则中心原子采用sp杂化,故C错误;
D.电负性越大,成键的键能越大越稳定,电负性:C<S<O,故分解温度:CS2、COS、CO2依次由低到高,故D正确.
故选D.
点评 本题考查化学键,注意把握习题中的信息为解答的关键,注意与二氧化碳的结构相似即可解答,侧重知识迁移应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.已知微粒的氧化性强弱:Br2>Fe3+>I2>S,判断下列反应不能发生的是( )
| A. | 碘化钾溶液与氯化铁溶液混和 2Fe3++2I-═2Fe2++I2 | |
| B. | 碘化亚铁溶液中滴入少量溴水Br2+2Fe2+═2Fe3++2Br- | |
| C. | 硫化钠溶液中加入足量的溴水Br2+S2-═S↓+2Br- | |
| D. | 硫化钠溶液加入少量氯化铁溶液 3S2-+2Fe3+═S↓+2FeS↓ |
12.下列叙述中正确的是( )
| A. | ${\;}_{17}^{37}$Cl的中子数为37 | B. | H2O与D2O互称同素异形体 | ||
| C. | NH3的电子式为 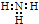 | D. | 1H与D互称同位素 |
9.H2有还原性,可以还原氧化铜,是因为H2中氢元素的化合价处于低价(0价),可以升高至+1价.由此分析:下列化学反应的反应物中的氢元素能体现还原性的是( )
| A. | Mg+2HCl═MgCl2+H2↑ | B. | 2Na2O2+2H2O═4NaOH+O2↑ | ||
| C. | NaH+H2O═NaOH+H2↑ | D. | 2H2O2═2H2O+O2↑ |
16.离子方程式Ba2++SO42-═BaSO4↓可表示下列反应中的:
①可溶性钡盐溶液与可溶性硫酸盐溶液之间的反应
②氢氧化钡溶液与可溶性硫酸盐溶液之间的反应
③稀硫酸与可溶性钡盐溶液之间的反应
④氢氧化钡溶液与稀硫酸反应.
说法正确的是( )
①可溶性钡盐溶液与可溶性硫酸盐溶液之间的反应
②氢氧化钡溶液与可溶性硫酸盐溶液之间的反应
③稀硫酸与可溶性钡盐溶液之间的反应
④氢氧化钡溶液与稀硫酸反应.
说法正确的是( )
| A. | ①② | B. | ①②④ | C. | ②③ | D. | ①③ |
13.关于对用惰性电极电解CuCl2溶液过程中的现象及本质的分析中正确的是( )
| A. | 所用电源可以直流电也可以是交流电 | |
| B. | 电解池工作过程中,阴离子移向阴极,阳离子移向阳极区 | |
| C. | 阳极区产生的气体可使湿润的KI-淀粉试纸变蓝色 | |
| D. | 若不考虑产物Cl2溶解产生的影响,则电解过程中溶液的浓度保持不变. |
 .
.