题目内容
【题目】有关晶体的结构如图所示,下列说法中不正确的是
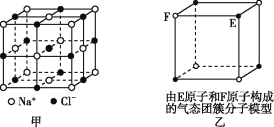
A. 在NaCl晶体(图甲)中,距Na+最近的Cl-形成正八面体
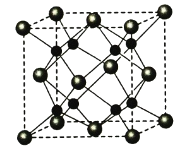
B. 该气态团簇分子(图乙)的分子式为EF或FE
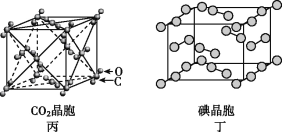
C. 在CO2晶体(图丙)中,一个CO2分子周围有12个CO2分子紧邻
D. 在碘晶体(图丁)中,存在非极性共价键和范德华力
【答案】B
【解析】
A项,如图甲所示,在NaCl晶体中,距Cl-最近的Na+有6个,同理距Na+最近的Cl-也有6个,这6个离子构成一个正八面体,故A正确;B项,如图乙所示,气态团簇分子中含有4个E原子,4个F原子,则分子式为E4F4或F4E4,故B错误;C项,如图丙所示,二氧化碳分子位于顶点和面心,且顶点和面心的距离最近,则每个顶点为12个面共有,一个CO2分子周围有12个CO2分子紧邻,故C正确;D项,如图丁所示,在碘晶体中碘分子之间存在范德华力,碘分子内两个碘原子间存在非极性共价键,故D正确。综上所述,符合题意的选项为B。

练习册系列答案
相关题目