题目内容
下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论或解释 |
| A | 向盛有0.5mol/L Fe(NO3)2溶液的试管中加入0.5mol/L H2SO4溶液 | 在试管口出现红棕色气体 | 溶液中NO3-被Fe2+还原为NO2 |
| B | 将一小块铝箔在酒精灯上加热 | 铝箔熔化却不滴落 | 氧化铝熔点高,包在铝的外面,所以熔化的铝不滴落 |
| C | 用醋酸溶液做导电性实验 | 灯泡较暗 | 醋酸是弱电解质 |
| D | 向浓度均为0.1mol?L-1NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.酸性条件下,亚铁离子与硝酸根离子发生氧化还原反应;
B.氧化铝的熔点高,包裹在Al的外面;
C.醋酸的浓度未知,导电性与离子浓度有关;
D.滴加少量AgNO3溶液,溶度积小的先沉淀.
B.氧化铝的熔点高,包裹在Al的外面;
C.醋酸的浓度未知,导电性与离子浓度有关;
D.滴加少量AgNO3溶液,溶度积小的先沉淀.
解答:
解:A.酸性条件下,亚铁离子与硝酸根离子发生氧化还原反应,溶液中NO3-被Fe2+还原为NO,然后NO被氧化为红棕色气体二氧化氮,故A错误;
B.氧化铝的熔点高,包裹在Al的外面,则铝箔熔化却不滴落,故B正确;
C.醋酸的浓度未知,导电性与离子浓度有关,则应利用等浓度的盐酸与醋酸进行对比性实验确定弱电解质,故C错误;
D.滴加少量AgNO3溶液,溶度积小的先沉淀,则出现黄色沉淀可知Ksp(AgCl)>Ksp(AgI),故D错误;
故选B.
B.氧化铝的熔点高,包裹在Al的外面,则铝箔熔化却不滴落,故B正确;
C.醋酸的浓度未知,导电性与离子浓度有关,则应利用等浓度的盐酸与醋酸进行对比性实验确定弱电解质,故C错误;
D.滴加少量AgNO3溶液,溶度积小的先沉淀,则出现黄色沉淀可知Ksp(AgCl)>Ksp(AgI),故D错误;
故选B.
点评:本题考查化学实验方案的评价,为高频考点,侧重分析能力与实验能力的综合考查,把握氧化还原反应、电解质的导电性实验、沉淀的生成及物质的性质为解答的关键,注意实验的评价性和操作性分析,题目难度不大.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案
相关题目
下列实验操作及结论正确的是( )
| A、使湿润的红色石蕊试纸褪色的气体一定是SO2 |
| B、量取8.58mL蒸馏水应选用10mL的量筒,而不能选用50mL的量筒 |
| C、检验氯代烃中含氯的方法是:向氯代烃中加入碱溶液,加热后先用稀硫酸酸化,再加入AgNO3溶液进行检验 |
| D、可用石墨作电极电解MgSO4和CuSO4的混合溶液,确定Mg和Cu的金属活动性强弱 |
下列实验操作正确的是( )
A、 检查气密性 |
B、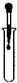 滴加试剂 |
C、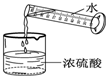 稀释浓硫酸 |
D、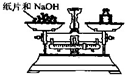 称量NaOH固体 |
金属及其制品在腐蚀介质中很容易被腐蚀,其使用寿命大为降低.因此只有对腐蚀介质中的金属及其制品采取防护措施,才能保证金属工艺设备的安全性和工农业生产的顺利进行.下面对金属及其制品的防护措施中错误的是( )
| A、铁锅用完后,用水刷去其表面的油污,置潮湿处保存 |
| B、通过特殊工艺,增加铝制品表面的氧化膜 |
| C、对于易生锈的铁制品(如防护网)要定期涂刷防护漆 |
| D、把Cr、Ni等金属加入到普通钢里制成不锈钢 |
某课外实验小组设计的下列实验不合理的是( )
A、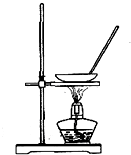 蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
B、 实验室制备少量氨气 |
C、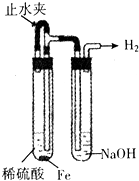 制备并观察氢氧化亚铁 |
D、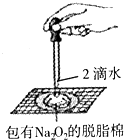 证明过氧化钠与水反应放热 |
下列物质中,既能与NaOH溶液又能与盐酸反应的氧化物是( )
| A、Al2O3 |
| B、Al |
| C、Al(OH)3 |
| D、NaHCO3 |
下列说法正确的是( )
| A、向蒸馏水中滴加浓H2SO4时,KW不变 |
| B、常温下,0.005mol?L-1 Ba(OH)2溶液pH为12 |
| C、Na2CO3水解的离子方程式为:CO32-+2H2O?H2CO3+2OH- |
| D、NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |