题目内容
右图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关的判断正确的是( )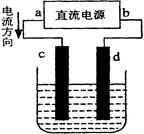
| A.b为正极、a为负极 | B.a为阳极、b为阴极 |
| C.电解过程中,d电极质量增加 | D.电解过程中,氯离子浓度不变 |
C
解析试题分析:电流从电源的正极经过用电器流回到电源的负极。A. 根据题图可知a的电源的正极,b是电源的负极。错误。B.与电源的正极a相连接的电极c为阳极,与电源的负极b相连接的电极d为阴极。错误。C.在电解过程中,由于阳离子的放电能力Cu2+>H+,所以在阴极发生反应:Cu2++2e-=Cu。产生的Cu附着在阴极d上,所以d电极质量增加。正确。D.在电解过程中,阴离子的沸点能力:Cl-> OH-,所以在阳极的电极反应式为:2Cl--2e-=Cl2 ↑。氯离子浓度会不断减小。错误。
考点:考查电解池中电极名称的判断及电极反应的应用的知识。

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
用铂电极电解100mL HNO3与 AgNO3的混合液,通电一段时间后,两极均收集到2.24 L 气体(标准状况),则原混合液中Ag+的物质的量浓度为 ( )
| A.1mol/L | B.2mol/L | C.2.5mol/L | D.3mol/L |
LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能的新宠。已知该电池放电时的电极反应式为:正极 FePO4+Li++e-==LiFePO4 负极 Li-e-="=" Li+下列说法中正确的是
| A.充电时电池反应为FePO4+Li = LiFePO4 |
| B.充电时动力电池上标注“+”的电极应与外接电的正极相连 |
| C.放电时电池内部Li+向负极移动 |
| D.放电时,在正极上是Li+得电子被还原 |
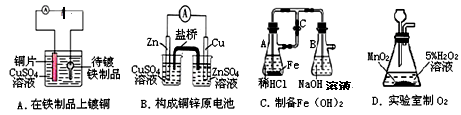
下列叙述中正确的是
| A.图①中正极附近溶液pH降低 |
| B.图①中电子由Zn流向Cu,盐桥中的Cl—移向CuSO4溶液 |
C.图②正极反应是O2+2H2O+4e¯ 4OH¯ 4OH¯ |
| D.图②中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀生成 |
以葡萄糖为燃料的微生物燃料电池结构如右图所示。a为电池的正极,关于该电池的叙述正确的是
| A.该电池能够在高温下工作 | B.b电极发生还原反应 |
| C.O2在a电极被氧化 | D.电流从a电极经用电器流向b电极 |
铜锌原电池(如右图)工作时,下列叙述正确的是
| A.在外电路中,电流从Zn极流向Cu极 |
| B.盐桥中的Cl-移向CuSO4溶液 |
| C.当负极减小65g时,正极增加65g |
| D.电池的总反应为 Zn + Cu2+=Zn2+ + Cu |
关于下列各装置图的叙述中,正确的是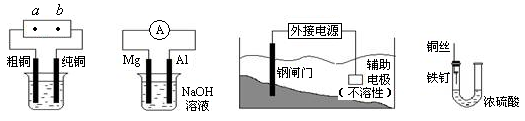
① ② ③ ④
| A.用装置①精炼铜,则a极为电源正极,电解质溶液为CuSO4溶液 |
| B.装置②中Mg为负极 |
| C.装置③中钢闸门应与外接电源的正极相连 |
| D.装置④中的铁钉被腐蚀 |
下列金属防腐的措施中,使用外加电流的阴极保护法的是
| A.水中的钢闸门连接电源的负极 |
| B.金属护拦表面涂漆 |
| C.汽车底盘喷涂高分子膜 |
| D.地下钢管连接镁块 |