题目内容
用铂电极电解100mL HNO3与 AgNO3的混合液,通电一段时间后,两极均收集到2.24 L 气体(标准状况),则原混合液中Ag+的物质的量浓度为 ( )
| A.1mol/L | B.2mol/L | C.2.5mol/L | D.3mol/L |
B
解析试题分析:在阳极上生成0.1molO2时,转移电子的物质的量为0.4mol,当阴极上生成0.1molH2时转移电子的物质的量为0.2mol,故银离子需得0.2mol电子,银离子的物质的量为0.2mol,浓度为2mol/L。
考点:电解的相关计算

练习册系列答案
相关题目
一种光化学电池的结构如下图,当光照在表面涂有氯化银的银片上时,AgCl(s) = AgCl(s)=" Ag" (s)+Cl(AgCl),[Cl(AgCl)表示生成的氯原子吸附在氯化银表面],接着Cl(AgCl)+e-—→Cl-(aq),若将光源移除,电池会立即回复至初始状态。下列说法正确的是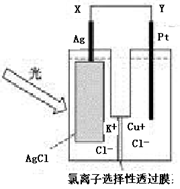
| A.光照时,电流由Y流向X |
| B.光照时,Pt电极发生的反应为2Cl-+2e-=Cl2 |
| C.光照时,Cl-向Ag电极移动 |
| D.光照时,电池总反应为:AgCl(s) + Cu+(aq)光Ag (s) + Cu2+(aq) + Cl—(aq) |
pH=a的某电解质溶液中,插入两只惰性电极,通直流电一段时间后,溶液的pH>a,则该电解质可能是 ( )
| A.H2SO4 | B.AgNO3 | C.Na2SO4 | D.NaOH |
钢铁发生吸氧腐蚀时,正极上发生的电极反应是 ( )
| A.2H++2e-=H2↑ | B.Fe2++2e-=Fe |
| C.2H2O+O2+4e-=4OH- | D.Fe3++e-=Fe2+ |
乙烯催化氧化成乙醛可设计成如图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应为:2CH2=CH2+O2→2CH3CHO。下列有关说法正确的是: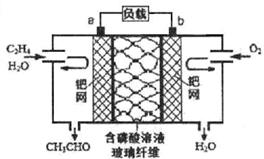
| A.该电池为可充电池 |
| B.每有0.1molO2反应,则迁移0.4mol |
| C.正极反应式为:CH2=CH2-2e-+2OH-=CH3CHO+H2O |
| D.电子移动方向:电极a→磷酸溶液 →电极b |
下列说法中正确的是
| A.在船体上镶嵌锌块,可以减缓船体被海水腐蚀的速率 |
| B.粗铜精炼时,电解液中的c(Cu2+)保持不变 |
| C.Na+的焰色反应呈黄色,属于化学变化 |
| D.在滴定实验中,可以用碱式滴定管量取21.0 mL的NaOH溶液 |
右图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关的判断正确的是( )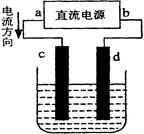
| A.b为正极、a为负极 | B.a为阳极、b为阴极 |
| C.电解过程中,d电极质量增加 | D.电解过程中,氯离子浓度不变 |
锂空气电池是一种新型的二次电池,其放电时的工作原理如图所示,下列说法正确的是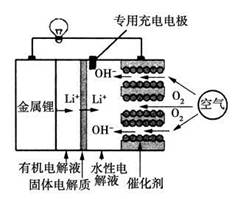
| A.该电池放电时,正极的反应式为O2+4e-+4H+===2H2O |
| B.该电池充电时,阴极发生了氧化反应:Li++e-===Li |
| C.电池中的有机电解液可以用稀盐酸代替 |
| D.正极区产生的LiOH可回收利用 |



