题目内容
【题目】(1)X是短周期中原子半径最小的元素,X、Y组成的气体甲能使湿润的红色石蕊试纸变蓝;
①Y的原子结构示意图是______________,甲的空间构型为__________。
②写出向硝酸铝溶液中通入过量气体甲的反应的离子方程式_________________。
(2)用硝酸铝溶液(加入分散剂)制备纳米氧化铝粉体的一种工艺流程如下。
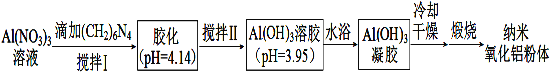
已知:①(CH2)6N4水溶液显碱性。
②Ksp[Al(OH)3] =1.3×10-33 ;溶液中离子浓度小于1×10-5 mol·L-1时,可认为这种离子在溶液中不存在。
凝胶中含有的硝酸盐除硝酸铝外还有___________________(填物质名称)。
(3)“拟晶”(quasicrystal)是一种具有凸多面体规则外形但不同于晶体的固态物质。某含铝“拟晶” 的化学式为:Al65Cu23Fe12, 它是二十世纪发现的几百种拟晶之一,具有合金的某些优良物理性能。下列有关这种拟晶的说法正确的是_______________。(填标号)
A.无法确定Al65Cu23Fe12中三种金属的化合价
B.Al65Cu23Fe12的硬度小于金属铁
C.Al65Cu23Fe12不可用作长期浸泡在海水中的材料
D.1 mol Al65Cu23Fe12溶于过量的硝酸时共失去265 mol电子
【答案】![]() 三角锥 Al3++3NH3+3H2O === Al(OH)3↓+3NH4+ 硝酸铵 C
三角锥 Al3++3NH3+3H2O === Al(OH)3↓+3NH4+ 硝酸铵 C
【解析】
(1)①X是短周期中原子半径最小的元素,是氢元素,X、Y组成的气体甲能使湿润的红色石蕊试纸变蓝,则甲为氨气,则Y是N元素,N的原子结构示意图是![]() ;氨分子的空间构型为三角锥形,故答案为:
;氨分子的空间构型为三角锥形,故答案为:![]() ;三角锥形;
;三角锥形;
②氨水与硫酸铝溶液反应生成氢氧化铝沉淀和硫酸铵,反应的离子方程式3NH3H20+Al3+=Al(OH)3↓+3NH4+,故答案为:3NH3H20+Al3+=Al(OH)3↓+3NH4+;
(2)硝酸铝加入(CH2)6N4水溶液充分搅拌,调节溶液pH=3.95时,可生成氢氧化铝胶体,水浴加热生成氢氧化铝凝胶,冷却、干燥后煅烧可得纳米氧化铝。因(CH2)6N4水溶液显碱性,-3价的N元素结合氢离子,+2价的CH2基团结合氢氧根离子,水解方程式为:(CH2)6N4+10H2O=6HCHO+4NH4++4OH-,则溶液中会存在硝酸铵,故答案为:硝酸铵;
(3)A、拟晶Al65Cu23Fe12是由三种金属元素组成,由于金属无负价,根据化合价代数和为0的原则,三种金属的化合价均可视作零价,错误;
B、拟晶具有合金的某些优良物理性能,合金的硬度一般比各成分金属大,错误;
C、Al65Cu23Fe12与海水可以构成原电池,会加速金属的腐蚀,因此不可用作长期浸泡在海水中的材料,正确;
D、溶于过量硝酸时,Al与Fe均变为+3价,Cu变为+2价,故1 mol Al65Cu23Fe12失电子为65×3+23×2+12×3=277 mol,错误。
故选C,故答案为:D。