题目内容
【题目】新型储氢材料是开发利用氢能的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为______,该能层具有的原子轨道数为_______。
②LiBH4由Li+和BH4-构成,BH4-的立体结构是_________,B原子的杂化轨道类型是________。
Li、B、H元素的电负性由大到小排列顺序为________。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径Li+_______H-(填“>”、“=”或“<”).
②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:

M是________ (填元素符号)。
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H-的半径为________,NaH的理论密度是___________g·cm-3(只列算式,不必计算出数值,阿伏加德罗常数为NA)
【答案】(1)①M;9;②正四面体;sp3;H>B>Li;
(2)①<;②Mg
(3)142pm![]()
【解析】
试题分析:(1)①基态Cl原子中电子占据的最高能层为第3能层,符号M,该能层有1个s轨道、3个p
轨道、5个d轨道,共有9 个原子轨道。
故答案为:M;9;
②BH4-中B原子价层电子数=4+![]() =4,B原子的杂化轨道类型是sp3杂化,且不含孤电子对,所以是正四面体构型,非金属的非金属性越强其电负性越大,非金属性最强的是H元素,其次是B元素,最小的是Li元素,所以Li、B、H元素的电负性由大到小排列顺序为H>B>Li。
=4,B原子的杂化轨道类型是sp3杂化,且不含孤电子对,所以是正四面体构型,非金属的非金属性越强其电负性越大,非金属性最强的是H元素,其次是B元素,最小的是Li元素,所以Li、B、H元素的电负性由大到小排列顺序为H>B>Li。
故答案为:正四面体;sp3;H>B>Li;
(2)①核外电子排布相同,核电荷数越大,离子半径越小,锂的质子数为3,氢的质子数为1,Li+、H-核外电子数都为2,所以半径Li+<H-。
故答案为:<;
②该元素的第III电离能剧增,则该元素属于第IIA族,为Mg元素。
故答案为:Mg;
(3)NaH具有NaCl型晶体结构,NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H-的半径为![]() =142pm,该晶胞中钠离子个数=8×
=142pm,该晶胞中钠离子个数=8×![]() +6×
+6×![]() =4,氢离子个数=12×
=4,氢离子个数=12×![]() +1=4,NaH的理论密度是ρ=
+1=4,NaH的理论密度是ρ=![]() =
=![]() 。
。
故答案为:142pm;![]() 。
。

【题目】硫酸铜晶体,俗称蓝矾、胆矾,具有催吐,祛腐,解毒。取5.0 g胆矾样品逐渐升高温度使其分解,分解过程的热重如下表。回答下列问题:
温度范围/℃ | 固体质量/g |
258~680 | 3.20 |
680~1000 | 1.60 |
1000以上 | 1.44 |
(1)测定蓝矾属于晶体的物理方法是____________。其中SO42-中S原子的轨道杂化形式是____________;H2O的空间构型是__________________。
(2)将硫酸铜晶体加热到258~680℃生成的物质A,A是__________(化学式);A溶于水配成溶液,加入氨水,观察到的现象是_____________________________________________;最终得到溶液中的含铜元素的离子是_________________(化学式),该离子含有的化学键类型有___________________。
(3)将硫酸铜晶体加热到1000℃以上生成的物质C,在C中的铜的离子的基态电子排布式是____________;
(4)如图是硫酸铜晶体分解得到一定温度的产物的晶胞(白球和黑球代表不同的原子)。
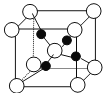
①该温度是_______________。
②铜原子的配位数是_______________。
③已知该晶体的密度为dg·cm-3,则晶胞参数是_________________pm。