题目内容
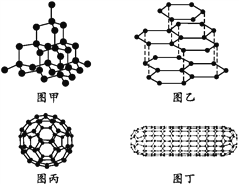
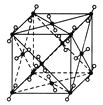
【题目】(1)如图为干冰的晶胞结构,观察图形,确定在干冰中每个CO2分子周围有________个与之紧邻且等距离的CO2分子。在干冰中撒入镁粉,用红热的铁棒引燃后,再盖上另一块干冰,出现的现象为____________________________,反应的化学方程式是__________________。
(2)下列三种晶体①CO2,②CS2,③SiO2的熔点由高到低的顺序是________>________>________(用序号填空),其原因是___________________________________________________。
【答案】 12 镁粉在干冰中继续燃烧,发出耀眼的白光,并有黑色物质生成 2Mg+CO2![]() 2MgO+C ③ ② ① SiO2是原子晶体,CO2、CS2是分子晶体,所以SiO2熔点最高;CO2和CS2组成和结构相似,且CS2的相对分子质量大于CO2的相对分子质量,所以CS2的熔点高于CO2
2MgO+C ③ ② ① SiO2是原子晶体,CO2、CS2是分子晶体,所以SiO2熔点最高;CO2和CS2组成和结构相似,且CS2的相对分子质量大于CO2的相对分子质量,所以CS2的熔点高于CO2
【解析】(1)干冰是分子晶体,二氧化碳分子位于立方体的顶点和面心上,以顶点上的二氧化碳分子为例,与它距离最近的二氧化碳分子分布在与该顶点相连接的12个面的面心上;镁粉在干冰内继续燃烧,发出耀眼的白光,有黑色固体生成;镁与二氧化碳在点燃的条件下反应生成氧化镁和碳,方程式2Mg+CO2![]() 2MgO+C;正确答案:12;镁粉在干冰中继续燃烧,发出耀眼的白光,并有黑色物质生成。
2MgO+C;正确答案:12;镁粉在干冰中继续燃烧,发出耀眼的白光,并有黑色物质生成。
(2)二氧化硅为原子晶体,熔点高,CO2和CS2为分子晶体,结构相似,相对分子质量越大熔点越高,所以三种物质的熔点顺序是③ >② >①正确答案:③、②、①; SiO2是原子晶体,CO2、CS2是分子晶体,所以SiO2熔点最高;CO2和CS2组成和结构相似,且CS2的相对分子质量大于CO2的相对分子质量,所以CS2的熔点高于CO2。

 53随堂测系列答案
53随堂测系列答案