题目内容
判断下列化合物中标出的显正价的元素正确的是( )
| A、OF2(F显正价) |
| B、CN-离子(N显正价) |
| C、NH3(H显正价) |
| D、SiC (C显正价) |
考点:化学键
专题:化学键与晶体结构
分析:根据在化合物中元素的正负化合价的代数和为0来解答即可.
解答:
解:A.F无正价,OF2中为-1价,氧为+2价,故A错误;
B.N的电负性大于C,CN-中C元素显+2价,N元素显-3价,故B错误;
C.N的电负性大于H,NH3中H元素显+1价,N元素显-3价,故C正确;
D.C的电负性大于Si,SiC中Si元素显+4价,C元素显-4价,故D错误.
故选C.
B.N的电负性大于C,CN-中C元素显+2价,N元素显-3价,故B错误;
C.N的电负性大于H,NH3中H元素显+1价,N元素显-3价,故C正确;
D.C的电负性大于Si,SiC中Si元素显+4价,C元素显-4价,故D错误.
故选C.
点评:本题考查元素化合价的计算,学生应熟悉常见元素在物质中的化合价,并能利用化合价的计算原则来进行简单计算.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羰基硫(COS),已知羰基硫分子中所有原子均满足八电子结构,结合周期表知识,有关说法不正确的是( )
| A、羰基硫分子为非极性分子 |
B、羰基硫的电子式为: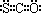 |
| C、羰基硫沸点比CO2高 |
| D、羰基硫分子中三个原子处于同一直线上 |
下列说法正确的是( )
| A、IA族元素的金属性比IIA族的元素金属性强 |
| B、第三周期元素的阴离子半径从左到右逐渐减小 |
| C、ⅥA族的气态氢化物一定比VA族的稳定性强 |
| D、原子晶体的熔点一定比离子晶体的高 |
下列分子中,所有原子的最外层均为8电子结构的是( )
| A、BeCl2 |
| B、H2S |
| C、光气(COCl2) |
| D、PCl5 |
下列实验现象描述错误的是( )
| A、H2在Cl2中燃烧发出苍白色火焰 |
| B、将S02通人品红溶液,溶液退色 |
| C、往稀硫酸中滴加酚酞试液,溶液变红色 |
| D、往淀粉溶液中滴加碘水,溶液显蓝色 |
下列说法正确的是( )
| A、HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 | ||||
| B、原子最外层电子数为2的元素一定处于元素周期表ⅡA族 | ||||
| C、NaOH和Na2O中所含的化学键类型完全相同 | ||||
D、
|
将2mol A和2mol B通入一密闭容器中,在某温度下达到平衡:2A(g)+B(g)?2C(g)+D(g).经测定,平衡时混合气体中C的体积分数为24%,则B的转化率为( )
| A、73% | B、24% |
| C、36% | D、12% |
NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、11g T216O含有的中子数为6NA |
| B、1mol Na2O2与CO2完全反应转移的电子数为2NA |
| C、1mol Na2O2固体中含离子总数为4NA |
| D、标准状况下,2.24L H2O所含共价键数为0.2NA |
 )有毒,不能用于制作食品保鲜袋.由氯乙烯通过加聚反应获得聚氯乙烯的化学方程式为:
)有毒,不能用于制作食品保鲜袋.由氯乙烯通过加聚反应获得聚氯乙烯的化学方程式为: