题目内容
在硫酸铜饱和溶液中加入m g无水硫酸铜粉末,维持温度不变,则析出固体物质质量为 .
考点:溶液中溶质的质量分数及相关计算
专题:计算题
分析:在硫酸铜饱和溶液中加入mg无水硫酸铜粉末,无水硫酸铜会吸收溶液中部分水分生成CuSO4?5H20,生成CuSO4?5H20的质量为mg×
=
mg,由于原饱和溶液中有部分溶剂减少,所以会析出部分硫酸铜,据此判断析出固体的质量.
| 250 |
| 160 |
| 25 |
| 16 |
解答:
解:无水硫酸铜的相对分子质量为160,CuSO4?5H20的摩尔质量为250g/mol,无水硫酸铜粉末融于水会吸水变成CuSO4?5H20,投入mg无水CuSO4后,析出的CuSO4?5H20的质量为:mg×
=
mg,由于CuSO4吸收了一部分水变成CuSO4?5H20,所以原先溶液中的溶质也有部分析出,析出的CuSO4的质量大于
mg,
故答案为:大于
mg.
| 250 |
| 160 |
| 25 |
| 16 |
| 25 |
| 16 |
故答案为:大于
| 25 |
| 16 |
点评:本题考查了饱和溶液特点、溶质质量分数的计算,题目浓度不大,注意明确饱和溶液的概念、溶质质量分数的计算方法,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
分子式为C5H11Cl的卤代烃发生消去反应生成的烯烃种数是( )
| A、3 | B、4 | C、5 | D、6 |
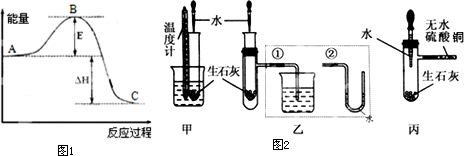
下列操作达不到预期目的是( )
①石油分馏时把温度计水银球插入受热的液体中;
②用酸性高锰酸钾溶液除去乙炔中含有的H2S;
③用溴乙烷在NaOH溶液中加热后,加入AgNO3溶液检验卤素原子;
④将苯和溴水混合后加入铁粉制取溴苯;
⑤将敞口久置的电石与蒸馏水混合制取乙炔.
①石油分馏时把温度计水银球插入受热的液体中;
②用酸性高锰酸钾溶液除去乙炔中含有的H2S;
③用溴乙烷在NaOH溶液中加热后,加入AgNO3溶液检验卤素原子;
④将苯和溴水混合后加入铁粉制取溴苯;
⑤将敞口久置的电石与蒸馏水混合制取乙炔.
| A、①⑤ | B、③④⑤ |
| C、①②③⑤ | D、①②③④⑤ |
Ag2Se单晶呈六角微型管状,有望开发为新型材料,其制取原理为:4AgCl+3Se+6NaOH═2Ag2Se+Na2SeO3+4NaCl+3H2O关于该反应下列叙述正确的是( )
| A、AgCl作氧化剂 |
| B、6mol NaOH参加反应转移6mol e- |
| C、氧化剂与还原剂的质量比为1:2 |
| D、被还原的元素与被氧化的元素的物质的量之比为2:1 |
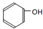 ;②
;②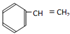 ;③
;③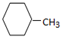 ;④
;④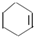 ;⑤
;⑤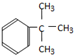 ;⑥
;⑥