题目内容
(1)1.8g的NH
离子中含有的电子数为 NA.
(2)常温常压下,48g O3含有的氧原子数为 NA.
(3)常温常压下,1.6g O2和O3所含氧原子数是 NA.
(4)1.806×1023个CO2所含氧原子数为 NA.
(5)如果a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是 .
(6)0.15mol/L 2L的Na2SO4溶液中含有SO42-的浓度是 mol/L.
(7)46g NO2和46g N2O4含有的原子数均为 NA.
(8)标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为 NA.
+ 4 |
(2)常温常压下,48g O3含有的氧原子数为
(3)常温常压下,1.6g O2和O3所含氧原子数是
(4)1.806×1023个CO2所含氧原子数为
(5)如果a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是
(6)0.15mol/L 2L的Na2SO4溶液中含有SO42-的浓度是
(7)46g NO2和46g N2O4含有的原子数均为
(8)标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为
考点:物质的量的相关计算,阿伏加德罗常数
专题:计算题
分析:根据n=
=
=
进行计算.
| m |
| M |
| N |
| NA |
| V |
| Vm |
解答:
解:(1)1.8g的NH
离子中含有的电子数为:
×10=1mol=NA,
故答案为:1;
(2)常温常压下,48g O3含有的氧原子数为:
=3mol=3NA,
故答案为:3;
(3)常温常压下,1.6g O2和O3所含氧原子数是:
=0.1mol=0.1NA,
故答案为:0.1;
(4)1.806×1023个CO2所含氧原子数为:
×2=0.6mol=0.6NA,
故答案为:0.6;
(5)如果a g某气体中含有的分子数为b,则c g该气体的物质的量为:
=
,标准状况下的体积是:
×22.4=
,
故答案为:
;
(6)0.15mol/L 2L的Na2SO4溶液中含有SO42-的浓度是:0.15mol/L,
故答案为:0.15;
(7)46gNO2和46gN2O4含有的原子数均为:
×3=3mol=3NA,
故答案为:3;
(8)标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为:
×2=1mol=NA,
故答案为:1.
+ 4 |
| 1.8 |
| 18 |
故答案为:1;
(2)常温常压下,48g O3含有的氧原子数为:
| 48 |
| 16 |
故答案为:3;
(3)常温常压下,1.6g O2和O3所含氧原子数是:
| 1.6 |
| 16 |
故答案为:0.1;
(4)1.806×1023个CO2所含氧原子数为:
| 1.806×1023 |
| 6.02×1023 |
故答案为:0.6;
(5)如果a g某气体中含有的分子数为b,则c g该气体的物质的量为:
| ||
| NA |
| bc |
| aNA |
| bc |
| aNA |
| 22.4bc |
| aNA |
故答案为:
| 22.4bc |
| aNA |
(6)0.15mol/L 2L的Na2SO4溶液中含有SO42-的浓度是:0.15mol/L,
故答案为:0.15;
(7)46gNO2和46gN2O4含有的原子数均为:
| 46 |
| 46 |
故答案为:3;
(8)标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为:
| 11.2 |
| 22.4 |
故答案为:1.
点评:本题考查物质的量的相关计算,难度不大.要注意平时基础知识的积累.

练习册系列答案
相关题目
下列离子方程式中,正确的是( )
| A、石灰石与醋酸反应:CaCO3+2H+=Ca2++CO2↑+H2O |
| B、氧化铁和稀硫酸反应:O2-+2H+=H2O |
| C、向NaHSO4溶液中加入过量的Ba(OH)2溶液:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D、向NaHCO3溶液中加入过量的Ba(OH)2溶液:Ba2++OH-+H++CO32-=BaCO3↓+H2O |
在托盘天平的左右两边各放一个烧杯,加入足量盐酸并使天平保持平衡向左边烧杯中加入14.4g Mg,向右边烧杯中加入14.4g Al,此时天平不再平衡,下述可以使天平恢复平衡的是( )
| A、右边加0.45g Al |
| B、左边加0.98g Mg |
| C、左边加14.4g Mg,右边加15.3g Al |
| D、左边加14.4g Mg,右边加14.85g Al |
下列氯化物中,既能由金属和氯气直接反应得到,又能由金属和盐酸反应制得的是( )
| A、FeCl2 |
| B、AlCl3 |
| C、FeCl3 |
| D、CuCl2 |
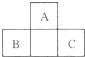 如图所示为短周期的一部分,如果B原子和C原子的核外电子总数之和为A的4倍,则:
如图所示为短周期的一部分,如果B原子和C原子的核外电子总数之和为A的4倍,则: