题目内容
在学习了铜元素的性质之后,小明同学做了H2O2与铜的有关探究实验:
实验一:将铜丝置于装有H2O2溶液的试管中,没有气体产生;加热溶液时,观察到铜丝表面产生大量气体。
实验二:将铜丝置于装有硫酸酸化的H2O2溶液的试管中,溶液迅速变蓝。同时产生大量气体。
请回答下列问题:
(1)上述实验一(加热时)、实验二中铜丝表面均产生了大量气体,该气体是 。
(2)写出在酸性条件下H2O2氧化铜丝的离子方程式: 。
(3)H2O2能发生多种化学反应,等物质的量的H2O2在仅作氧化剂的反应、仅作还原剂的反应和分解反应中转移的电子数目之比为 。
小明同学设计了以废铜屑制取硫酸铜的三个方案: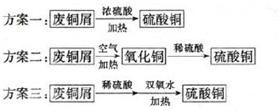
①认为最佳方案是 。
②简述另两个方案的不足之处: 。
(1)O2(2分)
(2)H2O2+2H++Cu=Cu2++2H2O(2分)
(3)2∶2∶1(2分)
(4)①方案二(1分)
②方案一生成的二氧化硫污染环境的同时会消耗更多的硫酸,方案三铜会催化过氧化氢的分解,增大成本(2分)
解析试题分析:(1)结合题意分析可知为:O2。
(2)H2O2+2H++Cu=Cu2++2H2O
(3)H2O2在仅作氧化剂的反应中-1价氧转变为-2价氧的得2电子、仅作还原剂的反应-1价氧转变为0价氧失去2电子,分解反应中-1价氧转移的1电子,等物质的量H2O2转移的数目之比为2∶2∶1。
(4)方案一生成的二氧化硫污染环境的同时会消耗更多的硫酸,方案三铜会催化过氧化氢的分解,增大成本,所以选择方案二。
考点:考察元素及其化合物性质、化学反应的计算。

今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Ca2+、Ba2+、CO32-、SO42-. 现取三份各100mL溶液进行如下实验:
第一份加入AgNO3溶液有沉淀产生;
第二份加入足量NaOH溶液加热后,收集到0.08mol气体;
第三份加入足量BaCl2 溶液后,得到干燥沉淀12.54g,经足量的盐酸洗涤、干燥后,沉淀质量为4.66g。
根据上述实验,回答以下问题:
(1)由第一份进行的实验推断该混合物是否一定含有Cl- : ,原因是 .
(2)由第二份进行的实验可知混合物中应含有 离子,其物质的量浓度为 .
(3)由第三份进行的实验可知12.54g 沉淀的成份为 。请计算形成该沉淀的原混合物中各离子的物质的量。(要求计算过程)
(4)综合上述实验,你认为以下结论正确的是
| A.该混合物中一定含有K+、NH4+、CO32-、SO42-,可能含有Cl-,且n(K+)≥0.04mol |
| B.该混合物中一定含有NH4+、CO32-、SO42-,可能含有Ca2+、 K+、Cl- |
| C.该混合物中一定含有NH4+、CO32-、SO42-,可能含有K+、Cl- |
| D.该混合物中一定含有NH4+、SO42-,可能含有Ca2+、K+、Cl- |
已知4℃时四种化合物在水中和液氨中的溶解度如下表:
| | AgNO3 | Ba(NO3)2 | AgCl | BaCl2 |
| H2O(液) | 170g | 9.2g | 1.5×10-4g | 33.3g |
| NH3(液) | 86g | 97.2g | 0.8g | 0g |
上述四种物质在水中形成复分解反应的离子方程式为 ,在液氨中形成复分解反应的化学方程式为 。
已知:还原性强弱:I― >Fe2+。往100 mL碘化亚铁溶液中缓慢通入3.36 L(标准状况)氯气,反应完成后溶液中有1/2的Fe2+被氧化成Fe3+。则原碘化亚铁溶液的物质的量浓度为
| A.1.1mol·L-1 | B.1.5mol·L-1 | C.1.2mol·L-1 | D.1.0mol·L-1 |


