题目内容
16.丁酸异戊酯又称香蕉油,多用于食品和化妆品的香精,实验室用正丁酸与异戊醇反应制备丁酸异戊酯,有关数据和装置示意图如下:CH3CH2CH2COOH+
 $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H20
+H20| 相对分子质量 | 密度(g/cm3) | 沸点(℃) | 水中溶解性 | |
| 正丁酸 | 88 | 0.9587 | 163.5 | 溶 |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 丁酸异戊酯 | 158 | 0.886 | 179 | 不溶 |

实验步骤:
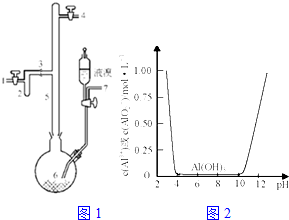
①如图1连接好装置,在三颈烧瓶中加入0.2mol异戊醇和0.1mol正丁酸、数滴浓硫酸、5mL苯和2~3片碎瓷片,充分摇匀,分水器内加入异戊醇直至与支管相平;
②在122~132℃下回流反应1.5h即可得粗产品;
③冷却后用10%的NaOH溶液中和,用水洗至中性,加入无水硫酸镁后蒸馏得较纯净的丁酸异戊酯11g.
回答下列问题:
(1)图1中A仪器的名称是球形冷凝管或冷凝管,冷却水应从a(选择a或b)口进.
(2)在该实验中,三颈烧瓶的容积最适合的是B(填入正确选项前的字母).
A、50mL B、100mL C、200mL
(3)加入碎瓷片的作用是防止暴沸;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是A(填入正确选项前的字母).
A、冷却后补加 B、立即补加 C、不需补加 D、重新配料
(4)加入过量异戊醇的目的是提高正丁酸的转化率,分离提纯过程中加入无水硫酸镁的目的是干燥.
(5)如图2,在蒸馏得较纯净的丁酸异戊酯操作中,仪器选择及安装都正确的是c(填标号).
(6)本实验的产率是69.6%.(保留三位有效数字)
分析 (1)根据仪器A的构造写出其名称;冷凝管的通水采用逆向通水法;
(2)根据反应物的物质的量计算出质量,再计算出需要各物质的体积,根据计算出的总体积判断需要三颈烧瓶的最佳容积;
(3)碎瓷片可以防止混合液在加热时发生暴沸现象;如果加热一段时间后发现忘记加碎瓷片,应冷却至室温,补加碎瓷片;
(4)正丁酸与异戊醇反应制备丁酸异戊酯的反应为可逆反应,根据反应物对化学平衡的影响分析加入过量异戊醇的作用;无水MgSO4的具有吸水性;
(5)根据温度计在蒸馏操作中的作用进行判断;
(6)根据产率=$\frac{实际产量}{理论产量}$×100%进行计算.
解答 解:(1)根据A的构造可知,仪器A为球形冷凝管或冷凝管;冷凝管采用逆向通水,冷凝效果较好,即:从a进水、b出水,
故答案为:球形冷凝管或冷凝管;a;
(2)0.2mol异戊醇的体积约为:$\frac{88g/mol×0.2mol}{0.8132g/mL}$≈21.6mL,0.1mol正丁酸的体积约为:$\frac{88g/mol×0.1mol}{0.9587g/mL}$≈9.2mL,还有5mL苯,混合液总体积大于:21.6mL+9.2mL+5mL=35.8mL,三颈烧瓶的容积应该为溶液体积的2倍左右,所以三颈烧瓶的最佳容积为100mL,所以B正确,
故答案为:B;
(3)混合液体加热时容易发生暴沸现象,所以加入碎瓷片可防止液体暴沸;液体加热要加碎瓷片,防止暴沸,如果加热一段时间后发现忘记加碎瓷片,应冷却至室温,补加碎瓷片,所以A正确,
故答案为:防止暴沸;A;
(4)酯化反应是可逆反应,增加一种反应物的物质的量可以提高另一种反应物的转化率,所以加入过量异戊醇可以提高正丁酸的转化率;无水MgSO4的具有吸水性,所以用无水MgSO4干燥丁酸异戊酯,
故答案为:提高正丁酸的转化率;干燥;
(5)在蒸馏操作中,温度计的水银球要放在蒸馏烧瓶的支管口处,所以ab错误,所以仪器及装置安装正确的是c,
故答案为:c;
(6)0.2mol异戊醇和0.1mol正丁酸反应,理论上可以生成0.1mol丁酸异戊酯,质量为:158g/mol×0.1mol=15.8g,而实际产量是11g,所以本次实验的产率=$\frac{11g}{15.8g}$×100%=69.6%,
故答案为:69.6%.
点评 本题考查性质实验方案的设计,涉及常见仪器的构造与安装、混合物的分离、提纯、物质的制取、药品的选择及使用、物质产率的计算等知识,题目难度较大,试题涉及的题量较大,知识点较多,充分培养了学生的分析、理解能力及灵活应用所学知识的能力,明确酯化反应原理及化学实验基本操作方法为解答关键.

 快乐5加2金卷系列答案
快乐5加2金卷系列答案| A. | CH3Br | B. | CH3CH2CH2CH2Br | C. | CH2BrCH2Br | D. | CH3CHBrCH2CH2Br |
| A. | 基态原子是处于最低能量状态的原子 | |
| B. | 基态C原子的电子排布式是1s22s12p3 | |
| C. | 焰色反应是金属原子的电子从基态跃迁到激发态时产生的光谱 | |
| D. | 同一原子处于激发态时的能量一定低于基态时的能量 |
| A. | 肯定存在① | B. | 至少存在②和⑤ | C. | 无法确定是否有③ | D. | 至少存在①、④、⑤ |
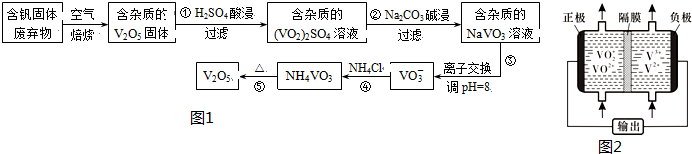
部分含钒化合物在水中的溶解性如表:
| 物质 | V2O5 | NH4VO3 | VOSO4 | (VO2)2SO4 |
| 溶解性 | 难溶 | 难溶 | 可溶 | 易溶 |
(1)反应①所得溶液中除H+之外的阳离子有VO2+和Al3+
(2)反应②碱浸后滤出的固体主要成分是Al(OH)3(写化学式).
(3)反应④的离子方程式为VO3-+NH4+=NH4VO3↓.
(4)25℃、101 kPa时,4Al(s)+3O2(g)═2Al2O3(s)△H1=-a kJ/mol
4V(s)+5O2(g)═2V2O5(s)△H2=-b kJ/mol
用V2O5发生铝热反应冶炼金属钒的热化学方程式是10Al(s)+3V2O5(s)=5Al2O3(s)+6V(s)△H=-$\frac{5a-3b}{2}$KJ/mol.
(5)钒液流电池(如图2所示)具有广阔的应用领域和市场前景,该电池中隔膜只允许H+通过.电池放电时负极的电极反应式为V2+-e-=V3+,电池充电时阳极的电极反应式是VO2+-e-+H2O=VO2++2H+.
(6)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应①后溶液中的含钒量,反应的离子方程式为:2VO+H2C2O4+2H+═2VO2++2CO2↑+2H2O.取25.00mL 0.1000 mol/LH2C2O4标准溶液于锥形瓶中,加入指示剂,将待测液盛放在滴定管中,滴定到终点时消耗待测液24.0mL,由此可知,该(VO2)2SO4溶液中钒的含量为10.6g/L.
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 70 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4•7H2O | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| 摩尔盐 | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
回答下列问题:
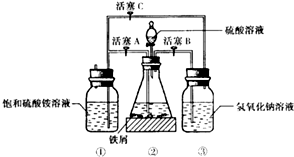
Ⅰ.(1)先用30%的氢氧化钠溶液煮沸废铁屑(含少量油污、铁锈、FeS等),再用清水洗净.用氢氧化钠溶液煮沸的目的是除去铁屑中油污
(2)将处理好的铁屑放人锥形瓶中,加入稀硫酸.锥形瓶中发生反应的离子方程式可能为ABCD(填序号).
A.Fe+2H+═Fe2++H2↑
B.Fe2O3+6H+═2Fe3++3H2O
C.2Fe3++S2-═2Fe2++S↓
D.2Fe3++Fe═3Fe2+
(3)利用容器②的反应,向容器①中通入氢气,应关闭活塞A,打开活塞BC (填字母).容器③中NaOH溶液的作用是吸收硫化氢气体,防止污染空气;向容器①中通人氢气的目的是防止亚铁离子被氧气氧化.
Ⅱ.待锥形瓶中的铁屑快反应完时,关闭活塞B、C,打开活塞A,继续产生的氢气会将锥形瓶中的硫酸亚铁(含极少部分未反应的稀硫酸)压到饱和硫酸铵溶液的底部.在常温下放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵.
硫酸亚铁与硫酸铵溶液混合就能得到硫酸亚铁铵晶体,其原因是硫酸亚铁铵的溶解度最小;从容器①中分离并得到纯净硫酸亚铁铵晶体的操作方法是过滤、用酒精洗涤、干燥.
Ⅲ.制得的硫酸亚铁铵晶体中往往含有极少量的Fe3+.为测定晶体中Fe2+的含量,称取一份质量为20.0g的硫酸亚铁铵晶体样品,制成溶液.用0.5mo1•L-1KMnO4溶液滴定,当溶液中Fe2+全部被氧化,MnO-4被还原成Mn2+时,耗KMnO4溶液体积20.00mL.
滴定时,将KMnO4溶液装在酸式(酸式或碱式)滴定管中,判断反应到达滴定终点的现象为溶液刚出现紫红色,保持30s不变;晶体中FeSO4的质量分数为38%.
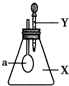 如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y.若挤压胶头滴管,使液体Y滴入锥形瓶中,振荡,过一会儿,可见小气球a鼓胀起来.气体X和液体Y不可能是( )
如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y.若挤压胶头滴管,使液体Y滴入锥形瓶中,振荡,过一会儿,可见小气球a鼓胀起来.气体X和液体Y不可能是( )| X | Y | |
| A | NH3 | H2O |
| B | SO2 | NaOH溶液 |
| C | CO2 | 6mol•L-1 H2SO4溶液 |
| D | HCl | 6mol•L-1 Na2SO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
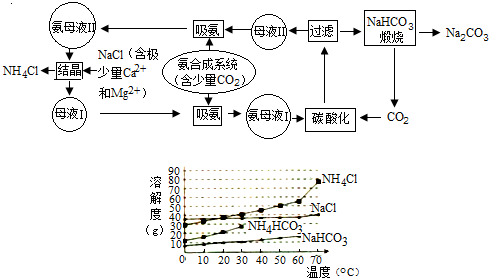
 利用废铝箔(主要成分为Al、少量的Fe、Si等)既可制取有机合成催化剂AlBr3又可制取净水剂硫酸铝晶体.
利用废铝箔(主要成分为Al、少量的Fe、Si等)既可制取有机合成催化剂AlBr3又可制取净水剂硫酸铝晶体.