��Ŀ����
����Ŀ����t��ʱ��Ag2CrO4(�ٺ�ɫ)��ˮ��Һ�еij����ܽ�ƽ��������ͼ��ʾ����֪AgCl��Ksp=1.8��10-10������˵������ȷ����
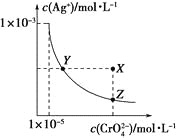
A.t ��ʱ��Ag2CrO4��KspΪ1��10-11
B.����Ag2CrO4��Һ�м���K2CrO4��ʹ��Һ��Y���ΪX��
C.t ��ʱ��Y���Z��ʱAg2CrO4��Ksp���
D.t ��ʱ����0.01mol��L-1AgNO3��Һ����20mL0.01mol��L-1KCl��0.01mol��L-1K2CrO4�Ļ����Һ�У�Cl-�ȳ���
���𰸡�B
��������
A����ͼ�����ݿɼ����Ksp[Ag2CrO4]��[Ag��]2��[CrO42��]��1.0��10��11����֪A��ȷ��
B����Ag2CrO4��Һ�м���K2CrO4��c(CrO42��)������c(Ag��)���ͣ���X����Y���c(Ag��)��ͬ������B����
C��Y�㡢Z����Һ���¶���ͬ����Ksp��ͬ��C��ȷ��
D����AgCl��Ksp�����������AgCl����ʱ��c(Ag��)��1.8��10��8mol��L��1����Ag2CrO4��Ksp�����Ag2CrO4����ʱ��c(Ag��)��3.16��10��5mol��L��1����֪Cl�����ȳ�����D��ȷ��
��ѡB��

��ϰ��ϵ�д�
�����Ŀ