题目内容
18.下列元素一定为主族元素的是( )| A. | 最外层有3个电子的元素 | B. | 最高正价为+7价的元素 | ||
| C. | 最外层电子数大于电子层数的元素 | D. | 内层电子数排满的原子 |
分析 A.最外电子层有3电子的元素,一定处于ⅢA族;
B.过渡元素中一些元素的最高正价可能为+7;
C.最外层电子数大于电子层数的元素可能为稀有气体元素;
D.内层电子数排满的原子可能为稀有气体元素、也可能为过渡元素.
解答 解:A.最外电子层有3电子的元素,一定处于ⅢA族,故A正确;
B.过渡元素中一些元素的最高正价可能为+7,故B错误;
C.如稀有气体最外层电子数是2或8,都大于电子层数,故C错误;
D.内层电子数排满的原子可能为稀有气体元素,如Ar,也可能为过渡元素,如Cu,故D错误,
故选A.
点评 本题考查结构性质位置关系应用,需要学生熟练掌握元素周期表的结构,注意利用列举反例法进行分析解答.

练习册系列答案
相关题目
20.人们研究金星大气成分,发现金星大气中有一种称之为硫化羰(COS)的分子,其结构与CO2类似,硫化羰是一种与生命密切相关的物质,下列有关COS的推测肯定不正确的是( )
| A. | COS分子是含有极性键的极性分子 | |
| B. | COS的电子式为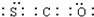 | |
| C. | COS分子中所有原子都满足8电子稳定结构 | |
| D. | COS属于离子化合物 |
9.下列相关的离子方程式书写正确的是( )
| A. | NaHS溶液水解:HS-+H2O?S2-+H3O+ | |
| B. | 向Ca(C1O)2溶液中通入SO2:SO2+2ClO-+H2O=SO32-+2HClO | |
| C. | 硫酸与氢氧化钡溶液混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| D. | 向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42ˉ刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3•H2O+H2O |
6.某有机物A是农药生产中的一种中间体,其结构简式如图.下列叙述正确的是( )


| A. | 有机物A属于芳香烃 | |
| B. | 有机物A能和Br2的CCl4溶液发生加成反应 | |
| C. | 有机物A和浓硫酸混合加热,可以发生消去反应 | |
| D. | 有机物A能和 NaOH乙醇溶液发生消去反应 |
3.下列与化学反应能量变化相关的叙述正确的是( )
| A. | 生成物总能量一定低于反应物总能量 | |
| B. | 放热反应在常温时即可发生,吸热反应必须加热才能发生 | |
| C. | 应用盖斯定律,可计算某些难以直接测量的反应焓变 | |
| D. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 |
7.对于H、D、T、H+四种符号的意义的下列描述正确的是( )
| A. | 表示同一种原子 | B. | 表示不同的原子 | ||
| C. | 表示同一种元素 | D. | 表示氢元素的4种同位素 |
8.2-溴丁烷与氢氧化钠的乙醇溶液共热反应的产物是( )
| A. | 1-丁烯 | B. | 2-丁烯 | C. | 1-丁醇 | D. | 2-丁醇 |

 (或写成
(或写成 R代表取代基或氢)
R代表取代基或氢) .
. .
.
 .
.