题目内容
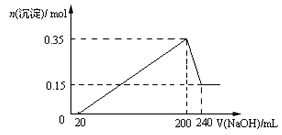
【题目】三氯氢硅(SiHCl3)是光伏产业的一种关键化学原料,制备反应的方程式为Si(s)+3HCl(g)![]() SiHCl3(g)+H2(g),同时还有其他副反应发生。当反应体系的压强为0.05 MPa时,分别改变进料比[n(HCl)∶n(Si)]和反应温度,二者对SiHCl3产率影响如图所示。下列说法正确的是
SiHCl3(g)+H2(g),同时还有其他副反应发生。当反应体系的压强为0.05 MPa时,分别改变进料比[n(HCl)∶n(Si)]和反应温度,二者对SiHCl3产率影响如图所示。下列说法正确的是
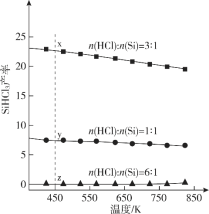
A. 降低压强有利于提高SiHCl3的产率
B. 制备SiHCl3的反应为放热反应
C. 温度为450 K,平衡常数:K(x)>K (y)>K (z)
D. 增加HCl的用量,SiHCl3的产率一定会增加
【答案】B
【解析】
A.Si(s)+3HCl(g)=SiHCl3(g)+H2(g)的反应正向为气体体积减小的方向,由于降低压强平衡向气体体积增大的方向移动,则对应此反应降低压强平衡向逆向移动,SiHCl3的产率会降低,故A错误;
B.如图所示,升高温度,曲线是向下倾斜的,即升高温度,SiHCl3的产率会降低,则升温平衡向逆向移动,逆向为吸热反应 ,则正向为放热反应,故B正确;
C.平衡常数与温度有关,温度不变,平衡常数是一个定值,则温度为450 K,平衡常数:K(x)=K (y)=K (z),故C错误;
D.如图所示,当n(HCl)∶n(Si)的进料比由1::1增大到3:1时,SiHCl3的产率是增加的,当增大到6:1时,SiHCl3的产率反而减小,故D错误。答案选B。

【题目】A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下:
元素 | 相关信息 |
A | 基态原子的价电子排布式为nSnnPn |
B | 元素原子的核外p电子数比s电子数少1个 |
C | 最外层电子数是电子层数的3倍 |
D | 简单离子是第三周期元素中离子半径最小的 |
E | 价电子层中的未成对电子数为4 |
请回答下列问题:
(1)写出下列元素的名称:A______, B_______, C________,D__________
(2)写出C元素在周期表的位置_________,E2+价电子的轨道表示式________________,B元素能量最高的电子为_____轨道上的电子,其轨道呈_______形.
(3)按原子轨道的重叠方式,1molA与C形成的最高价化合物中σ键有______个,π键有______个。
(4)B、C、D的简单离子的半径由大到小的顺序为_____________(用离子符号表示)。
(5)写出C的核外有18个电子的氢化物的电子式_____________。