题目内容
【题目】甲、乙两化学活动小组对中学化学教材中“氨的催化氧化”进行了实验探究。
(1)甲小组设计了如下图所示的实验装置(固定装置已略去)。

①若装置A中使用的药品是NH4HCO3固体,则A需要的仪器有试管、导管、橡胶塞和_______(填选项序号)。
a.锥形瓶 b.酒精灯 c.烧瓶 d.蒸发皿
②装置B的作用是___________________;装置D的作用是___________________。
③装置C中发生反应的化学方程式为________________________________。
④若A、B中药品足量,则可以观察到装置F中的实验现象是_____________________________。
⑤该装置存在的主要缺陷是___________________________________________________。
(2)乙小组认为可将甲小组的装置中A、B部分换成如图所示装置(其余部分相同)进行实验。

①烧瓶中加入的是过氧化钠固体,则分液漏斗中加入的最佳试剂是___________,U型管中加入的试剂是___________。
②此装置能产生大量氨气的原因是___________________________________________。
【答案】b 与水和二氧化碳反应,产生C中所需的反应物氧气 防止E中液体倒吸 4NH3+5O2 4NO+6H2O 铜片逐渐溶解,表面有气泡产生,溶液逐渐变蓝,液面上方气体逐渐变红棕色 F中液体可能会倒吸,尾气产生的NO2会污染环境 浓氨水 碱石灰(生石灰、氢氧化钠固体均可) 氨水中存在NH3+H2ONH3H2ONH4++OH-,Na2O2与水反应产生OH-并放出大量热量,使平衡左移,利于NH3释放
4NO+6H2O 铜片逐渐溶解,表面有气泡产生,溶液逐渐变蓝,液面上方气体逐渐变红棕色 F中液体可能会倒吸,尾气产生的NO2会污染环境 浓氨水 碱石灰(生石灰、氢氧化钠固体均可) 氨水中存在NH3+H2ONH3H2ONH4++OH-,Na2O2与水反应产生OH-并放出大量热量,使平衡左移,利于NH3释放
【解析】
本题主要考查实验探究,(1)A装置用于制取氨气和水,B装置用于制取氧气,C装置为反应装置,D装置防倒吸,E装置为干燥装置,F装置用于尾气吸收。(2)浓氨水与过氧化钠反应可产生实验所需氨气和氧气,据此分析。
(1)①若A中使用的药品是NH4HCO3固体,加热NH4HCO3固体需要酒精灯;
故答案为:b;
②装置B中盛放过氧化钠,碳酸氢铵受热分解生成NH3、CO2和H2O,过氧化钠和水、二氧化碳均反应生成氧气,氨气和氧气在催化剂作用下反应,所以装置B的作用是与水和二氧化碳反应,产生C中所需的反应物氧气;装置D作用是防止E中液体倒吸;
故答案为:与水和二氧化碳反应,产生C中所需的反应物氧气;防止E中液体倒吸;
③NH3与O2在催化剂、加热条件下发生反应生成一氧化氮和水,反应方程式为:![]() ;
;
故答案为:![]() ;
;
④若A、B中药品足量,生成的NO被氧化生成NO2,与水反应生成硝酸,硝酸能和铜反应生成硝酸铜和NO,反应现象为:铜片逐渐溶解,表面有气泡产生,溶液逐渐变蓝,液面上方气体逐渐变红棕色;
故答案为:铜片逐渐溶解,表面有气泡产生,溶液逐渐变蓝,液面上方气体逐渐变红棕色;
⑤该装置存在的主要缺陷是:F中液体因为压强变化的关系可能会倒吸,生成的二氧化氮有毒,应加一个尾气吸收装置;
故答案为:F中液体可能会倒吸,尾气产生的NO2会污染环境;
(2)①烧瓶中要产生氨气和氧气,则分液漏斗中加入的最佳试剂是浓氨水;干燥氨气和氧气可选用碱石灰(生石灰、氢氧化钠固体均可);
故答案为:浓氨水;碱石灰(生石灰、氢氧化钠固体均可);
②过氧化钠和氨水中水反应生成氢氧化钠和氧气,反应放热,氨水中存在NH3+H2ONH3H2ONH4++OH-,使平衡左移,利于NH3释放;
故答案为:氨水中存在NH3+H2ONH3H2ONH4++OH-,Na2O2与水反应产生OH-并放出大量热量,使平衡左移,利于NH3释放。

【题目】某同学对Cl2与KI溶液的反应进行了实验探究。反应装置如下:
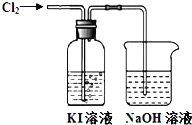
通入氯气一段时间,KI溶液变为黄色。继续通入氯气一段时间后,溶液黄色褪去,变为无色。继续通入氯气,最后溶液变为浅黄绿色。
(1)Cl2与NaOH溶液反应的化学方程式是___。
(2)KI溶液变为黄色说明氯气具有的___性,该反应的离子方程式是___。
(3)已知I2+I-![]() I3-,I2、I3-在水中均呈黄色。为确定黄色溶液的成分,进行了以下实验。
I3-,I2、I3-在水中均呈黄色。为确定黄色溶液的成分,进行了以下实验。
①实验b的目的是___。
②根据实验a中,水层中含有的粒子有___。
操作 | 实验现象 | |
a | 取2~3mL黄色溶液,加入足量CCl4,振荡静置 | CCl4层呈紫红色,水层显浅黄色 |
b | 取2~3mL饱和碘水,加入足量CCl4,振荡静置 | CCl4层呈紫红色,水层几近无色 |
③实验a中水溶液颜色变浅的原因是___。
④为保证实验的严谨性,在实验a、b的基础上,需补充一个实验,该实验为___。
(4)通入氯气,溶液由黄色变为无色,是因为氯气将I2氧化,已知1molCl2可氧化0.2molI2,该反应的化学方程式是___。
(5)根据上述实验,请预测向淀粉-KI溶液中持续通入氯气,可能观察到的现象为___。
(6)溶液最终变为浅绿色的原因是___。
【题目】A、B、C、D、E、F、G、H 是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
元素 | 相关信息 |
A | 原子核外有 6 种不同运动状态的电子 |
C | 基态原子中 s 电子总数与p 电子总数相等 |
D | 原子半径在同周期元素中最大 |
E | 基态原子最外层电子排布式为 3s23p1 |
F | 基态原子的最外层 p 轨道有两个电子的自旋方向与其他电子的自 旋方向相反 |
G | 基态原子核外有 7 个能级且能量最高的能级上有 6 个电子 |
H | 是我国使用最早的合金中的最主要金属元素 |
(1) A 元素的名称是_______________;A 元素和 F 元素形成的最简单化合物的分子构型为_______________,该分子是_______________分子。(填“极性”或“非极性”)
(2) B 元素形成的单质分子中σ键与π键数目之比为_______________。
(3) G 元素的低价阳离子的离子结构示意图是_______________。
(4) G 的高价阳离子的溶液与 H 单质反应的离子方程式为___________________________________