题目内容
2.下列事实不能用电化学理论解释的是( )| A. | 镁片不用特殊方法保存 | |
| B. | 镀锌的铁比镀锡的铁耐用 | |
| C. | 轮船水线以下的船壳上装一定数量的锌块以保护船体 | |
| D. | 纯锌与稀硫酸反应时,滴入少量硫酸铜溶液后速率加快 |
分析 电化学往往专门指“电池的科学”,因此事实中只要是形成了原电池则能用电化学理论解释.
A、Mg表面易形成致密的氧化物薄膜而阻止进一步的反应;
B、活泼性不同的两种金属遇到合适的电解质溶液能构成原电池,较活泼的金属作负极,负极易失电子被腐蚀;
C、活泼性不同的两种金属遇到合适的电解质溶液能构成原电池,较活泼的金属作负极,负极易失电子被腐蚀;
D、原电池原理可使反应速率加快;
解答 解:A、Mg表面易形成一层致密的氧化物薄膜而保护内层的镁不再被氧化,所以镁不用特殊方法保护,此现象与电化学知识无关,故A选;
B、镀锌铁发生金属被腐蚀现象时,因Zn比Fe活泼,Zn被腐蚀,镀锡铁破损后发生电化腐蚀,因Fe比Sn活泼,因而是铁被腐蚀.所以,镀锌铁比镀锡铁耐用.发生原电池反应而可用电化学知识解释,故B不选;
C、轮船水线下的船壳装上锌块后,可保护船壳在海水中不被腐蚀,因为Zn比Fe活泼,Zn与Fe构成原电池,在海水中锌被腐蚀,从而保护船壳,发生原电池反应可用电化学知识解释,故C不选;
D、滴入少量硫酸铜溶液后,锌把铜置换出来形成原电池反应,故加快反应速率,可用原电池原理解释,故D不选.
故选A.
点评 本题是对电化学知识的考查题,解题的关键是对相关的事实进行分析,只要是存在原电池的反应,便可用电化学理论解释.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
12.下列物质中碱性最强的是( )
| A. | LiOH | B. | NaOH | C. | Mg(OH)2 | D. | Al(OH)3 |
13.下列物质中既含有离子键又含有共价键的化合物是( )
| A. | NaCl | B. | N2 | C. | KOH | D. | SO2 |
10.丙烯醛的结构简式为CH2=CH-CHO.下列有关于它性质的叙述中错误的是( )
| A. | 能使溴水褪色,也能使高锰酸钾酸性溶液褪色 | |
| B. | 在一定条件下与H2充分反应,生成1-丙醇 | |
| C. | 能发生银镜反应表现出氧化性 | |
| D. | 在一定条件下能被空气氧化 |
17.下列观点中,错误的是( )
| A. | 化学反应既能实现物质的转化、又能实现能量的转化 | |
| B. | 分子是保持物质化学性质的一种粒子 | |
| C. | 储存在物质中的化学能在化学反应前后是不变的 | |
| D. | 构成宏观物质的微观粒子之间的相互作用有多种形式,如离子键、共价键等 |
14.下列说法中,正确的是( )
| A. | 苯、乙烯都能被酸性KMnO4溶液氧化 | |
| B. | 煤的干馏和石油的分馏原理相同,都是化学变化 | |
| C. | 从苯的凯库勒式看,分子中含有双键,所以苯属于烯烃 | |
| D. | 乙醇分子中的化学键如图,在Cu等催化作用下和O2反应,①③处断裂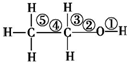 |
11.下列离子方程式中,书写正确的是( )
| A. | 碳酸氢钠溶液中加入过量的石灰水:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| B. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 用碳酸钠溶液吸收足量二氧化硫:2CO32-+2SO2+H2O═2HCO3-+SO32- | |
| D. | 在FeBr2溶液中通入足量的Cl2气体:3Cl2+2Fe2++4Br-═6Cl-+2Fe3++2Br2 |
12.已知Cl2、Br2、FeCl3、I2的氧化性依次减弱.下列反应不可能发生的是( )
| A. | Cl2+2H Br=2HCl+Br2 | B. | Cl2+FeI2=FeCl2+I2 | ||
| C. | 3Cl2+6FeI2=2FeCl3+4FeI3 | D. | 2Fe3++2I-=2Fe2++I2 |
 西南地区有较丰富的食盐矿和电力资源,适合建设大型的氯碱工业.下图是用惰性电极电解饱和食盐水的原理示意图,请回答下列问题:
西南地区有较丰富的食盐矿和电力资源,适合建设大型的氯碱工业.下图是用惰性电极电解饱和食盐水的原理示意图,请回答下列问题: